世界初の化学発光膜電位センサーの開発に成功。
| 原著論文 | Sci Rep 7, 42398 (2017) |
|---|---|
| 論文タイトル | Genetically encoded bioluminescent voltage indicator for multi-purpose use in wide range of bioimaging |
概要
大阪大学の稲垣成矩大学院生(生命機能研究科)と永井健治教授(生命機能研究科/産業科学研究所)らの研究グループは、細胞の電気シグナル(膜電位)を計測可能な化学(生物)発光膜電位センサーの開発に世界で初めて成功した。このセンサーを用いることにより、心臓病に対する薬剤評価や、脳の機能解明に役立つ事が期待される。
研究の背景
私たちの体において、膜電位変化を介した細胞間の情報伝達は非常に重要な役割を果たしている。特に心臓や脳といった器官は、そこに存在する細胞の膜電位変化が伝搬する事で、その高度な機能が維持されている。この膜電位変化の伝搬を計測する事は、特定の病気の原因究明や、その機能を解明する上で非常に重要であることが知られている。
同時に多くの細胞から膜電位情報を取得する上で、遺伝子にコードされた膜電位センサーは、非常に強力なツールである。現在まで、すべての膜電位センサーは蛍光タンパク質を利用しており、その膜電位依存的に増減する蛍光強度を計測する事で、細胞の膜電位変化を知ることができた。しかしながら蛍光を計測するために必要な励起光が強烈なため、しばしば細胞に対する光毒性や、蛍光タンパク質の光褪色を引き起こし、長時間計測を困難にしていた。また外部から光を照射する事で膜電位をコントロール可能な光遺伝学ツールは、神経科学の分野で広く使用されているが、膜電位センサーと共に用いる事で、励起光により誤って活性化してしまうといった問題があった。
本研究の成果
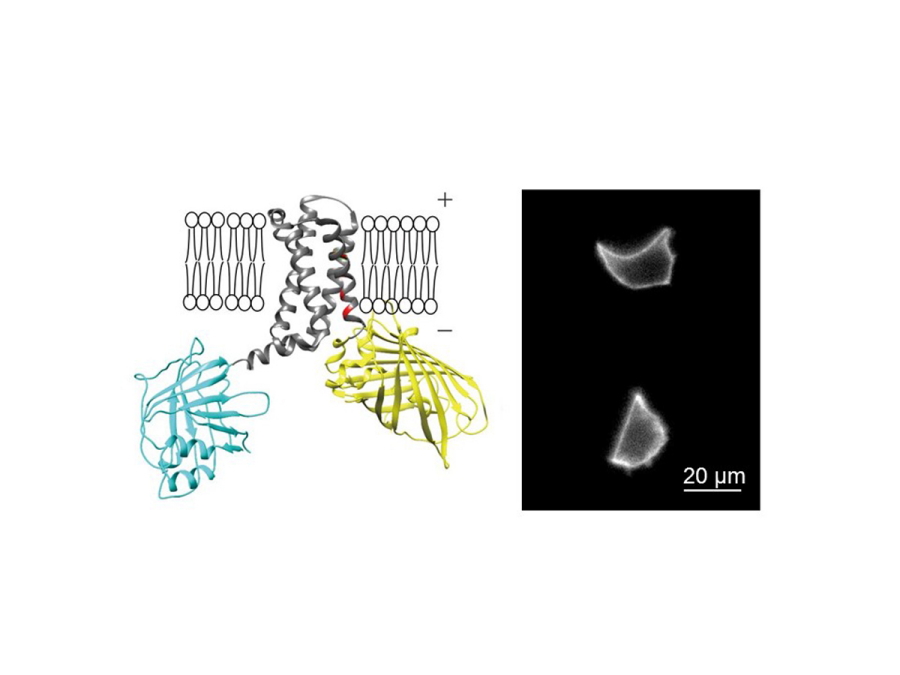
これらの問題を解決するために、稲垣成矩大学院生と永井健治教授らの研究グループは、基質を消費する事で発光可能な化学発光タンパク質に着目し、それを用いる事で、励起光照射が不要な化学発光膜電位センサーであるLOTUS-Vの開発に世界に先駆けて成功した(図1)。
また開発されたセンサーは励起光照射なしに細胞の膜電位を計測可能であるため、iPS細胞由来心筋細胞における膜電位変化を長時間観察可能である事や、培養細胞において複数の光遺伝学ツールと同時に組み合わせ可能である事を実証した。
研究成果のポイント
- 励起光照射なしに、細胞の電気シグナルを可視化できるセンサーの開発に成功
- チャネルロドプシン2などの光遺伝学ツールと自由に組み合わせ可能である事を実証
- iPS細胞由来心筋細胞におけるドラッグスクリーニングに役立つ事を実証
本研究成果が社会に与える影響(本研究成果の意義)
本研究は、世界に先駆けて励起光照射が不要な膜電位センサーであるLOTUS-Vを開発したことに意義がある。これにより従来の蛍光性膜電位センサーでは困難であった実験(複数の光遺伝学ツールと組み合わせた膜電位イメージング、長時間にわたる安定した計測)を容易にした点で、神経科学や創薬スクリーニングの分野に与える影響は非常に大きい。
今後の予定
今後はLOTUS-Vを用いて、自由行動マウスの脳活動を計測していく予定である。蛍光膜電位センサーの場合、光ファイバーを脳に挿入しなければならないのに対し、LOTUS-Vでは光ファイバーの挿入が不要なため、より簡便にかつ低侵略的に脳活動が計測できる事が予想される。
用語解説
- 膜電位
細胞内外でイオンの濃度に差がある事から生じる電位差のこと。 - 光毒性
強力な励起光を細胞に照射すると、細胞内で活性化酸素が生成される。その活性酸素が細胞にダメージを与える事を光毒性とよぶ。 - 光褪色
励起光を蛍光体に照射すると、一定の確率で構造が破壊され、蛍光を発しない状態になっていくこと。 - 励起光
蛍光体のエネルギー状態を励起させるために必要な、外部から照射する光の事。蛍光を観察するためには、必ず励起光を照射しなければならない。 - iPS細胞由来心筋細胞
体細胞に山中因子を導入し、分化万能性を持たせた細胞(iPS細胞)から分化誘導して作製された心筋細胞のこと
| 原著論文 | Sci Rep 7, 42398 (2017) |
|---|---|
| 論文タイトル | Genetically encoded bioluminescent voltage indicator for multi-purpose use in wide range of bioimaging |
| 著者 | Inagaki S (1), Tsutsui H (2, 3), Suzuki K (4), Agetsuma M (5), Arai Y (5), Jinno Y (3), Bai G (5), Daniels MJ (6), Okamura Y (1, 3), Matsuda T (5), Nagai T (1, 4, 5)
|
| PubMed | 28205521 |
