細菌の誘引行動と細胞内情報伝達の1細胞同時計測に成功
生物の好き嫌い行動のメカニズムを知る重要な手掛かりに
| 原著論文 | Science Advances 12(16):eaea7305, 2026 |
|---|---|
| 論文タイトル | Correlation of CheY-P concentration and motor behavior during attractant adaptation in single E. coli cells |
| 研究室サイト | 生体機能分子計測研究室〈石島 秋彦 教授〉 |
概要
大阪大学大学院生命機能研究科の福岡創准教授、石島秋彦教授らの研究チームは、大腸菌1細胞の誘引応答と細胞内の情報伝達を同時に観察することに成功しました。
大腸菌はとても小さな単細胞生物でありながら、走化性システムと呼ばれる情報伝達系でべん毛モーターの回転をコントロールし、好みの環境へ移動します(図1)。細胞外の刺激は細胞膜内の受容体で認識され、その情報はリン酸化された応答調節因子を通してべん毛モーターに伝えられ、細胞の運動がコントロールされます。大腸菌は好みの刺激(誘引刺激)を認識すると、ヒスチジンキナーゼの活性ならびに応答調節因子のリン酸化を抑制し、モーターの反時計回転を促します。その結果、細胞は誘引刺激に向かって直進遊泳します。また大腸菌は、一度反応した誘引刺激に反応しなくなるようにシステムをリセット(適応)して好みの環境に留まります。従来は大腸菌の誘引応答は、細胞の行動、あるいは細胞内のタンパク質動態についてそれぞれ個別に調べられてきました。しかし、実際に刺激に対して応答している細胞の中で、情報伝達を担う酵素がどのような動態を示すのか?それがどのような細胞行動に結びつくのかは不明でした。
今回、研究チームは、応答調節因子をYFP、応答調節因子の脱リン酸化酵素をCFPで蛍光標識し、両タンパク質間の蛍光共鳴エネルギー移動 (FRET) を計測することで、誘引刺激に対する応答調節因子濃度の変化と細胞の応答(べん毛モーターの回転)を同時に観察しました(図2)。その結果、べん毛モーターが誘引刺激による応答調節因子の濃度減少や、適応による濃度回復に鋭敏に応答すること、さらに応答調節因子濃度に対するモーターの感度が刺激受容前と刺激適応後で変化することをなど(図3)を、単一の生きた細胞で実証しました。これにより誘引応答時の応答調節因子の細胞内動態と細胞の行動を関連づけることができました。本成果は「細胞内の生体分子の振る舞いが生命の行動を生み出す根源的な原理」を知る重要な手掛かりになると期待されます。
研究の背景
大腸菌はとても小さな単細胞生物でありながら、走化性システムと呼ばれる情報伝達システムを使い、高等生物のように環境をモニターし、べん毛モーターの回転をコントロールしてより良い環境へ移動します(図1)。細胞外の刺激は細胞膜内の受容体で認識され、その情報はヒスチジンキナーゼによってリン酸化された応答調節因子を通してべん毛モーターに伝えられ、細胞の運動がコントロールされます。誘引刺激を受容すると、受容体はヒスチジンキナーゼを不活性化し、細胞外の誘引刺激の情報がヒスチジンキナーゼのリン酸化レベルの低下として細胞内の情報に変換されます。それに伴い応答調節因子のリン酸化が抑制され、モーターへ応答調節因子による情報が伝わらなくなります。その結果、べん毛モーターの反時計回転が持続し、細胞は誘引刺激に向かって直進遊泳します。その後、受容体はメチル化酵素によりメチル化され、ヒスチジンキナーゼの活性を誘引刺激前の状態に戻し、誘引刺激を打ち消します。この現象は適応とよばれます。この適応により、大腸菌は好みの環境に留まります。逆に受容体脱メチル化酵素はメチル化酵素と拮抗して忌避刺激を打ち消します。受容体はヒスチジンキナーゼなどの走化性関連タンパク質と共に、数万分子からなる巨大な受容体クラスターを形成しています。
これまで大腸菌の誘引応答は、細胞そのものの行動、あるいは細胞内のタンパク質動態のそれぞれについて個別に調べられてきました。しかし、実際に刺激に対して応答している細胞の中で、情報伝達を担うこれらの酵素がどのような動態を示すのか?その酵素の動態がどのような細胞行動に結びつくのかについては不明でした。
本研究の成果
本研究では、応答調節因子をYFPで、応答調節因子の脱リン酸化酵素をCFPで蛍光標識し、両タンパク質間の蛍光共鳴エネルギー移動 (FRET) を計測することで、生きた1つの細胞内で応答調節因子の濃度変化を観察できるようにしました。同時に、べん毛に付着させた微小なビーズを介して、応答調節因子の濃度変化と共にべん毛モーターの回転(細胞の応答)を同時に観察しました(図2)。
その結果、1)誘引刺激による応答調節因子濃度の減少と持続的なべん毛モーターの反時計回転、さらに2)適応による応答調節因子濃度の回復とモーター回転方向転換の再開を、生きた1細胞で実証することに成功しました。
細胞内の応答調節因子の濃度変化と細胞行動の詳細な解析により、1)べん毛モーターが誘引刺激による応答調節因子の濃度変化に鋭敏に応答すること(図2)、2)べん毛モーターは応答調節因子濃度に対する感度が誘引刺激の適応後で変化すること(図3)、などが実際の生きた細胞内で起こっていることがわかってきました。
以上のように、誘引刺激に対する細胞の行動と、その行動を制御する細胞内タンパク質の動態を、定量されたデータを基に関連づけることができました。
研究成果のポイント
- 大腸菌の誘引行動と情報伝達を担うタンパク質の細胞内動態を、同一の細胞かつ同時に計測することに成功し、両者の関係を定量化
- これまで細胞の行動と細胞内タンパク質の動態は別々に計測されており、両者の相関関係は同じ細胞で計測されていなかった
- 生体分子の振る舞いが生物の行動を生み出す原理」を知る重要な手掛かりとなり、生命に普遍的な好き嫌いの行動を生み出すメカニズムの分子レベルでの理解につながると期待
本研究成果が社会に与える影響(本研究成果の意義)
本研究は、外環境刺激に対する細菌の細胞内のタンパク質の動態と細胞行動の変化を同じ細胞で計測しており、細胞の中で行われている情報処理とそれにより生み出される細胞の行動を結びつけてとして理解することができるようになりました。これは『細胞内の生体分子の振る舞いが生物の行動を生み出す原理』を知る重要な手掛かりになります。大腸菌の走化性システムは真核生物の情報伝達システムにも共通する部分があるため、今後の研究によって生命に普遍的に存在する情報処理システム、特に好き嫌いの行動を生み出すメカニズムを考察する上でも重要な知見をもたらすと期待されます。
また大腸菌などの細菌は、有益な環境を認知し移動する、さらに有害な環境を感知し回避する高度な情報処理能力を備えています。今後、本研究で得られた知見をさらに発展させることで、病原細菌が宿主内でどのように移動し感染部位を選択しているのかという感染過程の理解だけでなく、将来的には細菌を直接殺傷するのではなく、その行動原理(忌避・走化性)を制御することで感染を抑制する治療法や予防法の創出が期待されます。
研究者のコメント
大腸菌は1つの細胞で生命として完結しています。今回の研究で、化学物質に対する細胞の応答行動の一端を、タンパク質の動態として理解することができるようになりました。今後も「細胞内の生体分子の振る舞いが生物の行動を生み出す原理」の解明を目指していきたいです。本研究で得られた知見をさらに発展させ、病原細菌が宿主内でどのように移動し感染部位を選択しているか?のような感染過程の理解や、細菌の行動原理を制御した感染を抑制法の創出などにもチャレンジしていきたいです。(福岡 創)
特記事項
本研究成果は、米国科学誌「Science Advances」(オンライン)に、2026年4月16日(木)午前3時(日本時間)に公開されました。
なお、本研究は、日本学術振興会(JSPS)科学研究費補助金JP25K0224、JP19H05797(研究代表者:石島秋彦)による支援を受けて行われました。
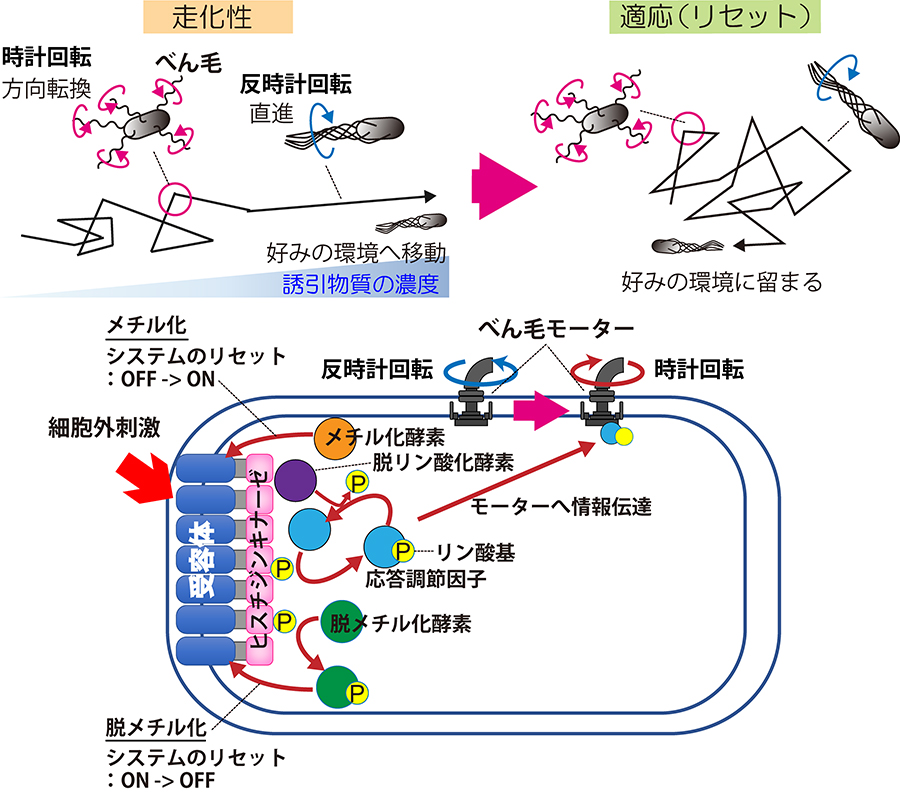
図1 大腸菌の走化性と走化性システムの情報伝達経路
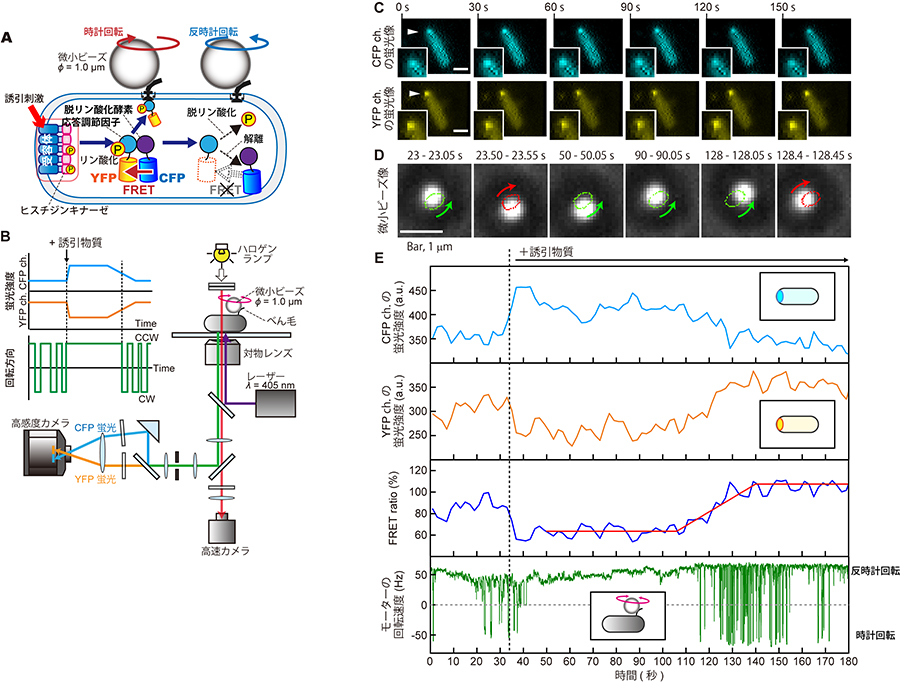
図2 誘引刺激に対する応答調節因子濃度変化と細胞応答の同時計測。
(A) 計測する細胞系。(B) 計測システム。(C) 結果の例。YFP標識した応答調節因子、CFP標識した脱リン酸化酵素を発現する細胞の蛍光像。(D) Cで示した細胞に付着させた微小ビーズ像。(E) CおよびDで示した細胞の蛍光強度、FRET割合、べん毛モーターの回転方向のそれぞれの時間変化。
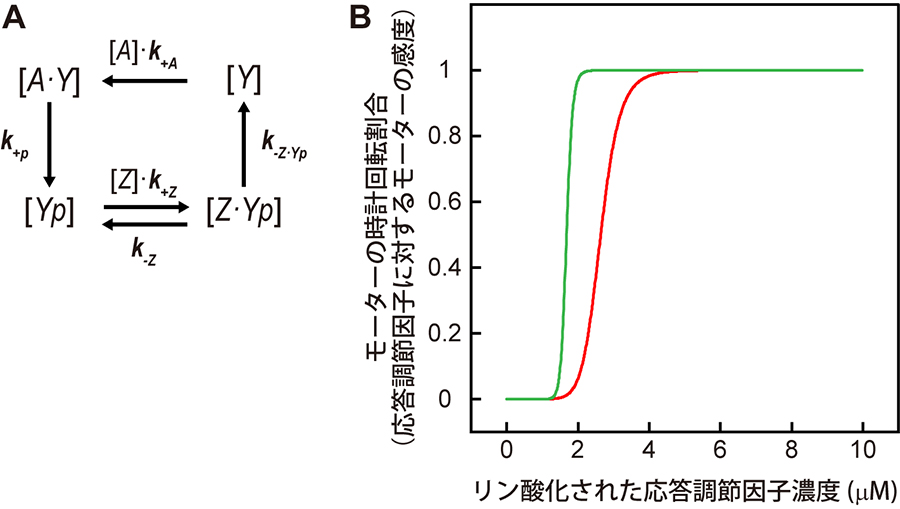
図3 刺激受容の前後におけるモーターの応答調節因子濃度に対する感度の変化。
(A) 応答調節因子のリン酸化状態における簡略化した速度論モデル。A、ヒスチジンキナーゼ:Y、応答調節因子:Yp、リン酸化された応答調節因子:Z、脱リン酸化酵素:k、それぞれの反応の速度定数。(B) 応答調節因子濃度に対するべん毛モーターの感度曲線。赤、誘引刺激前:緑、誘引刺激後。誘引刺激に適応後のモーターの方が応答調節因子濃度に対する感度が高くなっている。
用語解説
- 走化性システム
大腸菌が環境中の化学物質の濃度勾配に従って運動する走化性を示す。走化性システムはこの性質を制御する細胞内情報伝達系。細胞は誘引物質へ集まり、忌避物質には近づかない。 - べん毛モーター
大腸菌などの細菌の運動器官。タンパク質で作られた回転運動装置で、大腸菌のモーターは水素イオンをエネルギーとして回転する。 - 適応
一度反応した刺激に対して反応しなくなるようにシステムをリセットする機能。「適応」により大腸菌は広い範囲の濃度差を感知できる。 - YFP
黄色蛍光タンパク質 (Yellow Fluorescent Protein)。緑色の蛍光を発するタンパク質 (GFP) の遺伝子改変体で緑色光を吸収し黄色の蛍光を発する。観察したいタンパク質に融合させることで、細胞内で働くタンパク質を光らせて観察することができる。 - CFP
シアン蛍光タンパク質 (Cyan Fluorescent Protein)。GFPの遺伝子改変体で紫色光を吸収しシアン色の蛍光を発する。 - 蛍光共鳴エネルギー移動 (FRET)
Förster Resonance Energy Transfer。二つの蛍光分子の距離が非常に近く、かつ両者の向きが揃っている条件下において、ドナーの蛍光分子を励起した際に、ドナーのエネルギーがアクセプターの蛍光分子に移動し、ドナーの代わりにアクセプターが蛍光を発生する現象。本研究では応答調節因子が脱リン酸化酵素により脱リン酸化される際の両者の結合を、両者に融合させたCFPとYFP間のFRETにより検出している。FRETの変化からリン酸化応答された調節因子の細胞内濃度を推定することができる。
| 原著論文 | Science Advances 12(16):eaea7305, 2026 |
|---|---|
| 論文タイトル | Correlation of CheY-P concentration and motor behavior during attractant adaptation in single E. coli cells |
| 著者 | Tatsuya Yamakoshi, Yuki Takada, Takuma Nakagawa, Saki Ueda, Yumiko Uchida, Yong-Suk Che, Akihiko Ishijima, Hajime Fukuoka Graduate School of Frontier Biosciences, The University of Osaka, Suita, Osaka, Japan. |
| PubMed | 41984942 |
