新型コロナウイルスを中和するアルパカ抗体
オミクロンを含む全ての変異株に有効
| 原著論文 | Commun. Biol. 5(1):669 |
|---|---|
| 論文タイトル | A panel of nanobodies recognizing conserved hidden clefts of all SARS-CoV-2 spike variants including Omicron |
| 研究室サイト | 日本電子YOKOGUSHI協働研究所〈難波 啓一 特任教授(常勤)〉 |
概要
京都大学大学院医学研究科の高折晃史教授、大阪大学大学院生命機能研究科の難波啓一特任教授、藤田純三特任助教(常勤)、株式会社COGNANO(コグナノ)らの研究グループは、大阪大学感染症総合教育研究拠点/微生物病研究所、横浜市立大学、東京大学の研究グループとの共同研究により、新型コロナウイルスの「懸念される変異株(VOC:variant of concern)」である「オミクロン株(B.1.1.529, BA系統)」を含む全ての変異株に対して、これまで使用されてきたどの治療用抗体製剤よりも中和活性が高いナノボディ抗体を創出しました(図1)。さらに、クライオ電子顕微鏡を用いた立体構造解析から、これらのナノボディ抗体は新型コロナウイルス表面に存在するスパイクタンパク質の深い溝をエピトープにしていることが示されました。このエピトープはヒトの抗体が到達できない部分であり、ウイルスの変異がほとんど見られない領域です(図2)。また、これらのナノボディ抗体は新型コロナウイルスへの結合力が極めて強く、環境安定性も高いため、下水などの環境中のウイルスを濃縮し、検出する用途にも応用することができます。
研究の背景
新型コロナウイルス感染症(COVID-19)は、2年半以上経った2022年7月現在においてなお完全な収束には至らず、これまでに世界でおよそ7億人が感染し、700万人が亡くなりました。新型コロナウイルス(SARS-CoV-2)は、変異を繰り返して広まり、現在主流である「オミクロン株」は、それまでのVOC(アルファ株、ベータ株、ガンマ株、デルタ株)と比べて、スパイク蛋白の変異箇所が圧倒的に多く、以前感染した人やワクチン接種者にも感染します。また、オミクロン株による新型コロナウイルス感染症には、その出現前に開発された治療用抗体のほとんどが効かなくなることが明らかになっています。
本研究の成果
我々は、免疫したアルパカ遺伝子から最適な創薬候補をコンピュータで選択する独自技術をもとに、オミクロン株を含む全ての変異株に対して、これまで使用されてきたどの治療用抗体製剤よりも中和活性が高いナノボディ抗体の樹立に成功しました。さらに、クライオ電子顕微鏡を用いた立体構造解析から、これらのナノボディ抗体が、新型コロナウイルスの表面に存在するスパイクタンパク質の深い溝をエピトープにしていることを示しました。このエピトープはヒトの抗体が到達できない部分であり、ウイルスの変異がほとんど見られない領域です。
研究成果のポイント
- 現在パンデミックの主流となっている「オミクロン株」を中和するナノボディ抗体を樹立しました。
- オミクロン株は、ワクチンによって誘導された中和抗体や治療用抗体製剤から逃避します。本研究で創られた抗体は、これまでに報告されたいずれの中和抗体よりも高い有効性を示しました。
- 本研究で創られたアルパカ抗体は、ヒト抗体の10分の1の大きさです。そのため、ヒト抗体が到達できないスパイクタンパク質の深い溝に入り込むことができます。その様子をクライオ電子顕微鏡により撮像し、構造解析により証明することができました。
- 本抗体は環境耐性が高く、全ての新型コロナウイルス変異株を検出できます。そのため、下水など環境中のウイルスの濃縮やモニタリングにも利用することができます。
本研究成果が社会に与える影響(本研究成果の意義)
ワクチンで誘導される中和抗体や、これまでに開発された治療用抗体は、新型コロナウイルス上のスパイクタンパク質の表面に結合して感染を抑えるものが多いです。より小型のナノボディ抗体は、スパイクタンパク質の表面よりも奥まった深い溝(本論文では「クレバス」または「隠された裂け目」と呼んでいます)に結合できます。この深い溝には、ヒトの抗体は大きすぎて入り込むことができず、宿主による抗体免疫系の選択圧がかからないため、新型コロナウイルスのほぼ全ての変異株において、変異の見られない共通の構造をしています。これらの知見は、大阪大学大学院生命機能研究科の難波啓一特任教授、大阪大学大学院薬学研究科の井上豪教授、大阪大学感染症総合教育研究拠点の松浦善治拠点長・特任教授(常勤)/微生物病研究所兼任の研究グループが、日本電子株式会社(JEOL)との共同研究において得ることができました。このような稀少な有用抗体を計算科学を用いて探索する方法は、COGNANO社が世界で初めて開発したものです。
また、ナノボディ抗体は遺伝子工学による改変がしやすく、ヒト抗体よりも数千倍安価に生産できます。京都大学医学研究科高折晃史教授の研究グループは、本研究で得られた知見に基づき、より中和活性の高い改変ナノボディ抗体を作成し、臨床応用を目指しています。
現在、京都大学、大阪大学、COGNANO社では、さまざまな感染症について、ウイルス学的な解析や、中和抗体やナノボディ抗体の構造解析についての研究に取り組んでおり、新型コロナウイルスのみならず、エイズウイルス(HIV)、ネコエイズウイルス、サル痘、その他、がん免疫を明らかにするための研究を推進しています。
特記事項
本研究成果は2022年7月6日に英国科学雑誌「Communications Biology」にオンライン掲載されました。
なお、本研究は、高折晃史教授らに対する日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業(JP20fk0108268、JP20fk0108517)、ポプリ薬局、難波啓一特任教授らに対するAMED創薬等先端技術支援基盤プラットフォーム(BINDS: JP21am0101117)、AMED医療研究開発革新基盤創成事業(CiCLE: JP17pc0101020)、日本電子(JEOL)YOKOGUSHI協働研究所、科学研究費補助金(JP25000013)、藤田純三特任助教に対する科学研究費補助金(JP20K22630)、井上豪教授らに対する科学技術振興機構(JST)産学共創プラットフォーム共同研究推進プログラム(OPERA: JPMJOP1861)、株式会社COGNANOに対する京都府助成金・京都産業21(産学公の森)、神奈川県衛生研究所などの支援の下で実施されました。
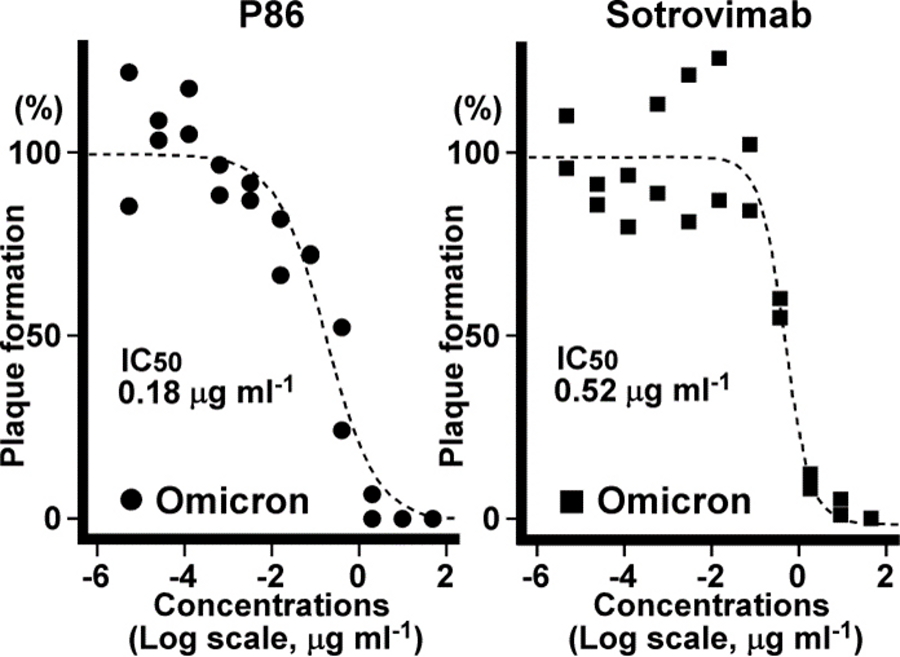
図1.ナノボディ抗体(P86)のオミクロン株(BA.1)への中和活性
現存の治療抗体の中で唯一オミクロン株に対して中和活性を示すソトロビマブ抗体よりも強い活性(低いIC50値)を示す。
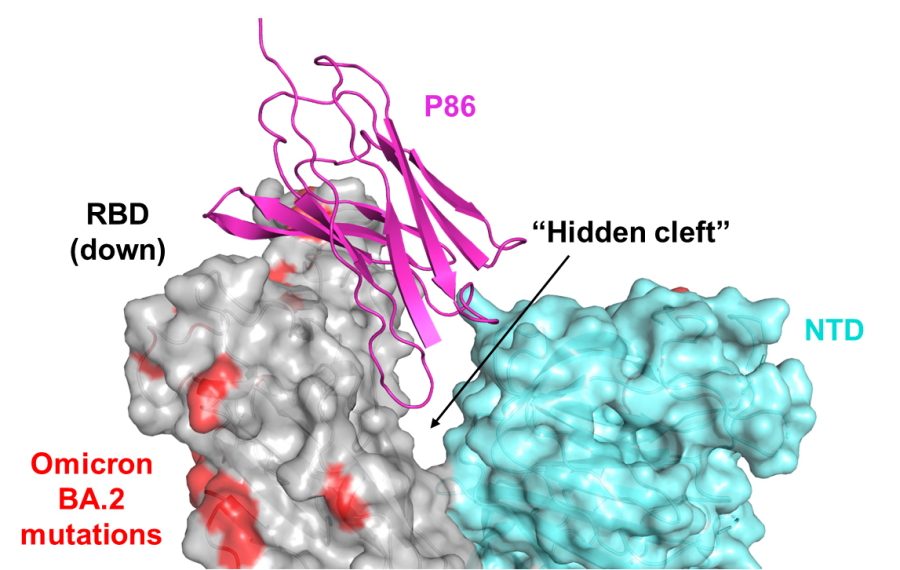
図2.スパイクタンパク質にナノボディ抗体が結合した構造
ナノボディ抗体(P86)が結合している深い溝(または隠された裂け目)にはオミクロン株(BA.2)における変異箇所(赤色で示す)が存在しない。
用語解説
- オミクロン株(B.1.1.529, BA系統)
世界保健機構により、2021年11月に5つ目のVOCに認定され、世界各国で大流行しており、現在パンデミックの主たる原因となる変異株となっている。 - ナノボディ抗体
別名VHH抗体。ラクダ科の動物(アルパカなど)とサメ科の動物が持つ重鎖のみからなる特殊な抗体。ヒトや他の動物の抗体は、重鎖と軽鎖からなるより複雑で大きな分子となっている。 - クライオ電子顕微鏡
生体分子を極低温下で観察し、構造解析を行うために用いられる電子顕微鏡。世界では日本電子社製とサーモフィッシャー製(米国)がシェアを分けている。2017年ノーベル化学賞受賞につながった。日本では日本電子株式会社が、難波啓一大阪大学特任教授、藤吉好則東京医科歯科大学特別栄誉教授らのグループとの共同研究で開発し、今回の成果にも日本電子社製のクライオ電子顕微鏡CRYO ARMTM 300が活用された。また、大阪大学の井上豪教授、難波啓一特任教授の両研究グループが共同で独自開発したEG-grid(酸化修飾グラフェングリッド)もこの成果に貢献した。グラフェン表面を特殊な化学反応で酸化、化学修飾して観察対象分子をグリッド上に高密度吸着させることにより、クライオ電子顕微鏡像データ収集の大幅な高速化を可能にした。 - エピトープ
抗体が結合する生体分子のある特定の部位。エピトープが変異したウイルスは、抗体による免疫系を逃れることができる。 - 環境安定性が高い
ナノボディ抗体は、水質の温度・湿度・酸性アルカリ性・有機物・金属含有量などに対して、活性を保てる範囲が通常の抗体よりも広いことが知られている。 - 中和抗体
ウイルスや細菌の感染から身を守る抗体のこと。ワクチン接種によって誘導される。また、治療用抗体としても用いられている。
| 原著論文 | Commun. Biol. 5(1):669 |
|---|---|
| 論文タイトル | A panel of nanobodies recognizing conserved hidden clefts of all SARS-CoV-2 spike variants including Omicron |
| 著者 | Ryota Maeda (1, 2), Junso Fujita (3, 4), Yoshinobu Konishi (1), Yasuhiro Kazuma (1), Hiroyuki Yamazaki (2, 5), Itsuki Anzai (6), Tokiko Watanabe (6), Keishi Yamaguchi (4), Kazuki Kasai (2), Kayoko Nagata (1), Yutaro Yamaoka (7), Kei Miyakawa (7), Akihide Ryo (7), Kotaro Shirakawa (1), Kei Sato (8, 9, 10), Fumiaki Makino (3, 11), Yoshiharu Matsuura (12, 13), Tsuyoshi Inoue (4), Akihiro Imura (2), Keiichi Namba (3, 14, 15), Akifumi Takaori-Kondo (1)
|
| PubMed | 35794202 |
