植物ホルモンを使って動物細胞を操る技術
人工オーキシンでさらにパワーアップ
| 原著論文 | Nucleic Acids Res. 48(18):e108 (2020) |
|---|---|
| 論文タイトル | A super-sensitive auxin-inducible degron system with an engineered auxin-TIR1 pair |
| 研究室サイト | 染色体生物学研究室〈深川 竜郎 教授〉 |
概要
大阪大学大学院生命機能研究科の深川竜郎教授らの研究グループは、名古屋大学大学院理学研究科の西村浩平助教(元深川研究室特任助教)、嘉村巧教授ら、名古屋大学トランスフォーマティブ生命分子研究所の鳥居啓子教授、萩原伸也准教授(現理化学研究所チームリーダー)、打田直行特任准教授(現名古屋大学遺伝子実験施設教授)、高橋宏二助教との共同研究で、タンパク質の機能解析に重要となる人工オーキシンを用いた高感受性タンパク質分解系を確立しました。
生物を構成する細胞の中では様々なタンパク質が機能することにより、生命現象が維持されています。細胞の中の特定のタンパク質の役割を知るには、そのタンパク質を細胞内から除去し、細胞に現れる表現型を解析する方法が一般的です。これまで標的とするタンパク質を細胞内から速やかに分解・除去するシステムとして、植物ホルモン・オーキシンを用いたオーキシンデグロン法が知られており、世界中で用いられています。
今回、研究グループは人工的に改変したオーキシン分子とその受容体のペアを用いることで、従来のオーキシンデグロン法よりも1000倍も高感受性をもつオーキシンデグロン法(Super-sensitive AID system)の開発に成功しました。この方法では標的タンパク質の分解に必要なオーキシンの量を従来の1000分の1にまで減少させることができるため、オーキシン自身の細胞毒性を低く抑えることができます。この方法はマウスやヒトの様々な細胞で機能することから、今後、これらの細胞でタンパク質の速やか、かつ低毒性な分解系として様々なタンパク質の機能解析や創薬での利用が期待されます。
研究の背景
生物を構成する細胞の中では様々なタンパク質が遺伝子産物として働き、生命現象を維持しています。このようなタンパク質の機能を解析する方法として、ノックアウトマウスなどのように遺伝子を破壊して、細胞にどのような影響が現れるかを解析する方法があります。しかし、遺伝子の中には細胞の増殖に必須な遺伝子も存在しており、こうした遺伝子を破壊すると細胞が増殖できなくなってしまい、解析することができません。そのため、このような遺伝子の解析には、特定の条件によって、自分たちが壊したい標的タンパク質(遺伝子産物)を分解・除去する系が利用されています。オーキシンデグロン法は、植物ホルモンであるオーキシンを分解誘導剤として用いることにより、標的とするタンパク質を速やかに分解する系(Nishimura et al., Nature Methods, 2009)であり、酵母からヒトの細胞に至るまで、さまざまな生物種において、遺伝子の機能解析に利用されてきました。しかしながら、動物の培養細胞では分解誘導剤として使用するオーキシンの濃度は非常に高く、時として、細胞にダメージを与えてしまうこともありました。
本研究の成果
分解誘導剤として用いるオーキシンの量を減らすために、従来よりも高感度なオーキシンデグロン法の構築を試み、その際に名古屋大学トランスフォーマティブ生命分子研究所で開発された人工オーキシンと受容体のペアに注目しました。この人工オーキシンと受容体のペアはbump-and-hole法という手法を用いて設計されており、従来のオーキシンと受容体のペアよりも1000倍以上も高感受性であることがわかっていました(図1)。この人工オーキシンと受容体のペアを用いたオーキシンデグロン法では従来のものと比べて、わずか1/1000の量のオーキシンで標的タンパク質の分解を誘導することができました(図2)。
この高感度オーキシンデグロン法がどのような細胞で働くかを調べるため、一般的な研究で用いられる種々の細胞を用いて、染色体分配において機能する因子の分解誘導を行いました。すると、マウスES細胞をはじめとする様々な動物の培養細胞において、低濃度の人工オーキシンによる因子の分解が確認されました(図3左)。さらに、これらの細胞では染色体の分配異常による細胞増殖という表現型も確認することができました(図3右)。以上の結果はこの高感度オーキシンデグロン法が様々な動物の培養細胞で機能することを示しています。
研究成果のポイント
- 人工的に改変したオーキシン分子とその受容体を用いて従来よりも1000倍も高感度なオーキシンデグロン法を開発しました。
- 高感度なオーキシンデグロン法がマウスやヒトの様々な細胞で機能することを示しました。
- 今後、様々なタンパク質を標的として速やかに分解・除去することにより、タンパク質の機能解析や創薬での利用が期待されます。
本研究成果が社会に与える影響(本研究成果の意義)
この方法では標的タンパク質の分解に必要なオーキシンの量を従来の1000分の1にまで減少させることができるため、オーキシン自身の細胞毒性を低く抑えることができます。さらに、マウスやヒトをはじめとする様々な真核生物細胞で用いることが可能と考えられるため、今後、これらの細胞でタンパク質の速やかなかつ低毒性な分解系として様々なタンパク質の機能解析や創薬での利用が期待されます。
特記事項
本研究成果は、2020年9月17日付(英国時間)英国科学雑誌「Nucleic Acids Research」のオンライン版に掲載されました。
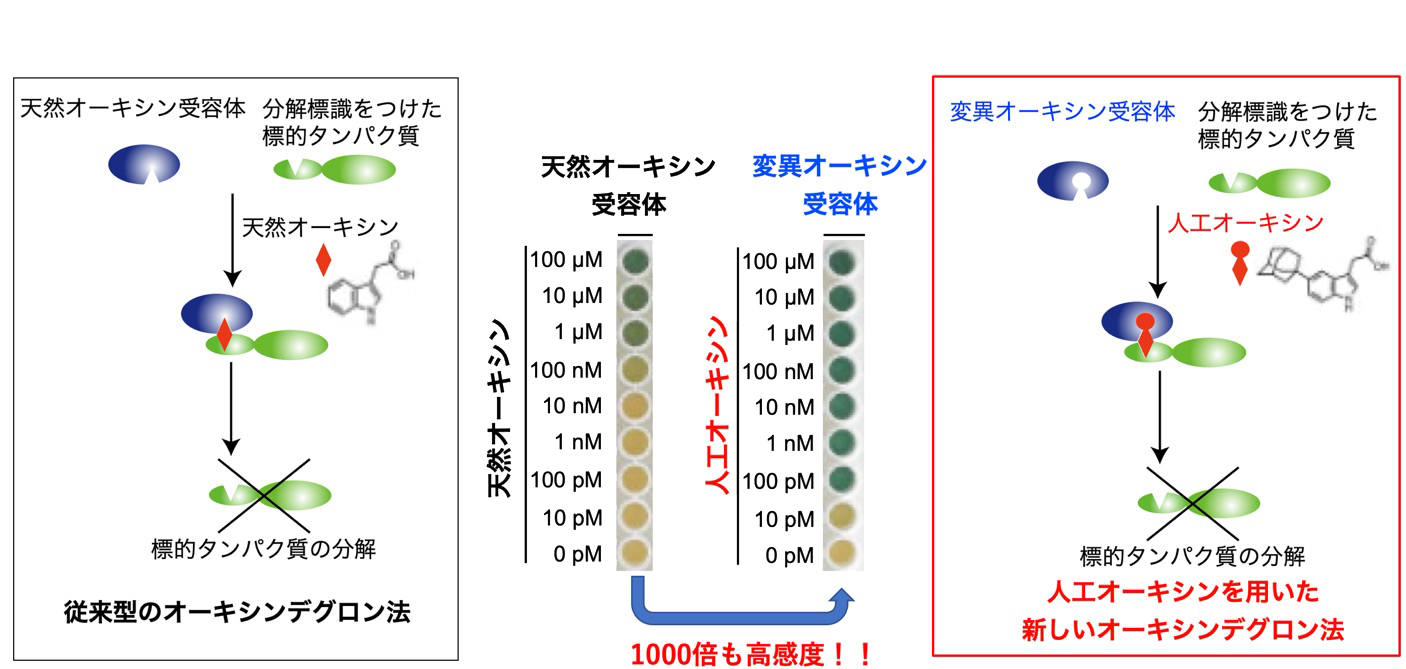
図1.人工オーキシンと受容体を利用したオーキデグロン法
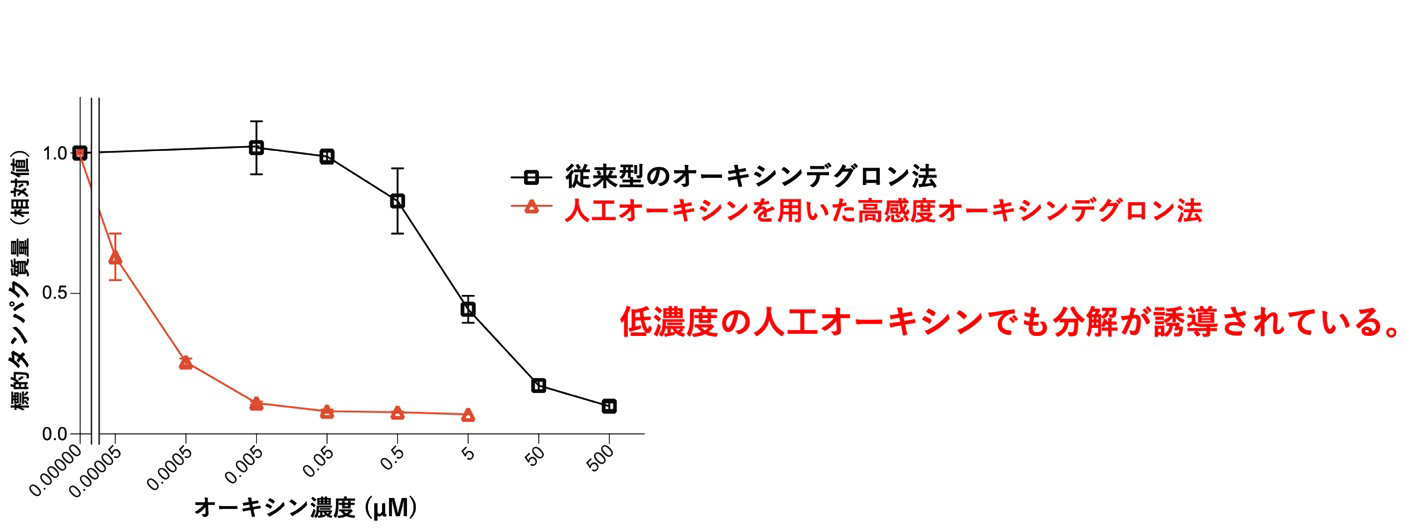
図2.ルシフェラーゼを用いたタンパク質分解実験
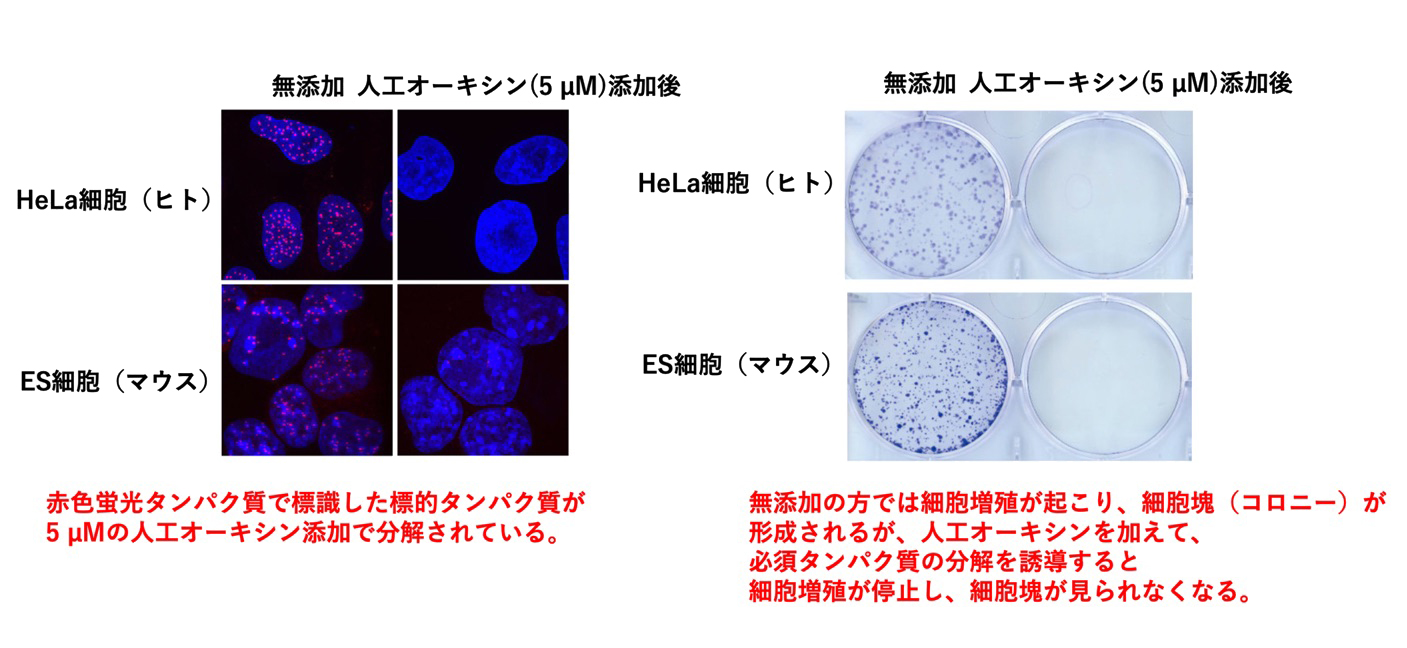
図3.ヒトやマウスの細胞における必須タンパク質の分解とその表現型
| 原著論文 | Nucleic Acids Res. 48(18):e108 (2020) |
|---|---|
| 論文タイトル | A super-sensitive auxin-inducible degron system with an engineered auxin-TIR1 pair |
| 著者 | Kohei Nishimura (1, 2), Ryotaro Yamada (3, 6), Shinya Hagihara (3, 6), Rie Iwasaki (3), Naoyuki Uchida (3, 7), Takumi Kamura (2), Koji Takahashi (2, 3), Keiko U. Torii (3, 4, 5), Tatsuo Fukagawa (1)
|
| PubMed | 32941625 |
