マウス性決定遺伝子Sryの全貌をついに解明
Sryに隠れた暗号コードが存在、性決定を支配する因子はまさしくコレだ!!
| 原著論文 | Science 370(6512):121-124 (2020) |
|---|---|
| 論文タイトル | The mouse Sry locus harbors a cryptic exon that is essential for male sex determination |
| 研究室サイト | エピゲノムダイナミクス研究室〈立花 誠 教授〉 |
概要
大阪大学大学院生命機能研究科の宮脇慎吾招へい教員、立花誠教授らの研究グループは、マウスの性決定遺伝子Sryにはこれまで知られていなかった“隠れエキソン”が存在し、そのエキソンは真の性決定因子であるSRY-Tをコードしていることを世界で初めて明らかにしました。
ほ乳類の性決定遺伝子であるSryは、性決定因子であるSRYタンパク質をコードしています。SRYが胎仔期の生殖腺で発現することで、ほ乳類のオス化が始まります。これがほ乳類の性決定の仕組みです。Sryが発見されてから30年もの間、Sryはひとつのエキソンで構成され、ただ一種類のSRYのみをコードすると考えられていました。
今回、立花教授らの研究グループは、性が決まる時期のマウスのトランスクリプトームを解析することにより、Sryにはこれまで見過ごされてきた第2エキソン(隠れエキソン)が存在し、この隠れエキソンこそが新規の性決定因子であるTwo-exon type SRY(SRY-T)をコードしていることを発見しました。この隠れエキソンをゲノム編集により欠損させたオスのマウスはメスへと性転換しました。また逆に、SRY-Tを強制発現させたメスのマウスはオスへと性転換しました(図1)。これらの実験により、SRY-Tが生体内で必要かつ十分な性決定因子であることが証明されました。この発見は、ほ乳類の性決定の仕組みの解明と、性決定遺伝子の進化の理解につながることが期待されます。
研究の背景
哺乳類にはオスとメスの性があります。どのように性が決まるのかは古代ギリシア時代より議論されており、性決定の研究分野は生物学の大きなテーマのひとつです。ほ乳類の性は性染色体の組み合わせで決まることが知られています。XX型はメスになり、XY型はオスになります。1991年にKoopmanらのグループにより、Y染色体に存在するSryが性決定遺伝子であると示されました。すなわち、Y染色体を有していれば、Sryが活性化することでその個体はオスになります。Sryが発見されて以降の30年間、「Sryは、単一のエキソンで構成される遺伝子(単一エキソン遺伝子)であり、たった一種類のタンパク質SRYをコードする」と考えられてきました。これは教科書的事実として認知され、誰も疑いを挟みませんでした。
本研究の成果
Sryの隠れたエキソンを発見
今回、立花誠教授らのグループは、マウスを使った実験で、Sryの新たなエキソンを発見しました。本グループは、これまでにSryが発現する細胞を選択的に集める方法を確立していました。その方法を用いて、Sryが発現する細胞の網羅的遺伝子発現解析(RNA-seq)をした結果、Sryの近傍に未知の転写産物が存在することに気がつきました。マウスのSry遺伝子座には、Sryを挟んで左右で完全に同じ配列が鏡写しに存在するパリンドローム構造があります。通常の解析方法ではパリンドローム構造に隠されて未知の転写産物は表示されません。パリンドローム構造を想定した解析方法により、はじめて未知の転写産物が描出されます(図2)。次に、転写開始点を網羅的に解析する手法(CAGE-seq)や、転写されたRNAを長い状態のまま網羅的に解析する手法(long-read RNA-seq)などの最新の手法を用いて解析した結果、この未知の転写産物がSryの第2のエキソン(隠れエキソン)であることを明らかにしました。
Sry-Tはオスの性決定に必要・十分である
次に、Sry-Tの性決定における役割を調べるために、Sryの第2エキソンをゲノム編集により削除したSry-T欠損マウスを作製しました。Sry-T欠損マウスはSry-Sを発現しているにもかかわらずメスに性転換しました(図3)。このことからSry-Tはオスへの性決定に必須であることが明らかになりました。さらに、今回発見したSry-Tとこれまでに知られていたSry-Sを、XX型のマウスで活性化させると、Sry-Tを活性化させたマウスのみがメスからオスへ性転換しました(図3)。以上の実験から、生体では、これまでに知られていたSRY-Sではなく、SRY-Tが性決定因子として働いていることが明らかになりました。
SRY-Sにはオス化能力を不十分にするタンパク質分解シグナル(デグロン)が存在する
次に、Sry-Sは実験的にマウスをオス化する能力を持つにもかかわらず、生体ではオス化できない原因を調べました。SRY-SとSRY-Tのアミノ酸配列を比べると、後方のアミノ酸配列が異なります。この違いを解析した結果として、デグロンと呼ばれるタンパク質を分解する配列がSRY-Sにのみ存在することが分かりました。デグロンの最後から2番目のアミノ酸をバリンからプロリンに変えると、デグロンは不活性化されます。そこで、SRY-Tの欠損に加えてSRY-Sの最後から2番目のアミノ酸をバリンからプロリンに置換したマウスを作製したところ、SRY-Sタンパク質の分解が抑えられ、このマウスはオスになりました。以上の実験から、SRY-Sは自身のデグロン配列によりタンパク質が不安定になり、生体でのオス化能力がないことがわかりました。Sry-Sを用いた過去の実験では、タンパク質の不安定化を補えるほど多くのSry-Sを発現させることによって、オスにすることができたと考えられます。
Sry-Tはデグロンを回避するために進化した?
一方で、今回の発見は性決定遺伝子の進化においても、新しい知見をもたらしました。Sryが存在するY染色体は進化の過程でどんどん遺伝子を失っていることが知られています。これは、Y染色体以外の染色体は互いに修復が可能な対となる染色体を持っていますが、Y染色体は1本しか存在せず、遺伝子の修復ができないためだと考えられています。このように、ほ乳類のY染色体は、様々な遺伝子の機能が失われていく危機に直面していると考えられています。今回我々が見つけたSry-Sのデグロンをコードしている配列も、遺伝子の機能が失われる危機のひとつと考えられます。Sryの“隠れエキソン”は、レトロトランスポゾン由来の配列で構成されています(図4)。このことは、レトロトランスポゾン由来の配列がエキソン化することでデグロン配列を回避させた、すなわちSryの機能消失の危機を救ったと考えられます。これはウイルスに由来する配列が宿主の遺伝子を進化させ、その種の存亡の危機を救った可能性を示しており、ウイルスと宿主生物との関係について、改めて考えさせる研究結果となりました。
研究成果のポイント
- ほ乳類の性決定遺伝子Sryが発見されて以来、Sryは単一エキソンの遺伝子だと30年間信じられてきた。今回、マウスSryには隠れた第2のエキソンが存在し、それは新規の性決定因子であるSRY-Tタンパク質をコードしていた。
- これまでに知られていた単一エキソン型の性決定因子SRY-Sは、マウスのメスをオスに性転換させることが難しかった。一方で、我々が見つけた新規性決定因子、SRY-Tは、効率よく性転換させることができた。このことから、SRY-Tがマウスの真の性決定因子であることが明らかになった。
- SRY-Sは、タンパク質分解をうける機能不全型であるが、第2エキソンがコードするSRY-Tは安定型であり、生体内で真の性決定因子として働くことを明らかにした。
- 本研究は、ほ乳類の性決定の仕組みの解明と、性決定遺伝子の進化の理解に繋がる。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、生物学の大きなテーマのひとつである性決定において、鍵となる重要な遺伝子Sryの全体像が解明されました。この発見はほ乳類の性決定の仕組みの解明と、性決定遺伝子の進化の理解につながると期待されます。今後、他の生物におけるSRY-Tや、SRY-Sのデグロンの存在を検証していきます。また現在、立花誠教授が研究代表を務める新学術領域「性スペクトラム」では、生物の性を連続する表現型(スペクトラム)として捉え直し、性に関する様々な現象の統一的な説明に挑戦する試みがなされています(http://park.itc.u-tokyo.ac.jp/sexspectrum/)。今回の研究成果は、マウスの性スペクトラムを規定する因子の再定義につながりました。これまで築きあげられたSry-Sによる研究成果が見直され、今後はSry-Tをキープレイヤーとした性の仕組みの理解が進むと期待されます。
今から10数年ほど前、Sryを含むY染色体上の遺伝子は退化の一途を辿り、オスはやがていなくなるだろうとの考え方が提唱されました。今回の私たちの発見は、このような考え方に一石を投じるものです。私たちの研究成果は、オス化に関わる最も重要な遺伝子が現在進行形で進化していることを意味しているからです。
研究者のコメント
研究を始めた当初、Sryに第2のエキソンが存在することは全く予想ができず、未知の転写産物はノンコーディングRNAやエンハンサーなのではないかと考えていました。その可能性を検証するためにCAGE-seqの結果を解析し、研究室のメンバーと議論をしたところ、予想とは違う結論に至り落胆しました。しかしながら、RNA-seqのデータを再度慎重に見返すと、あまたあるデータの中でたった1本のリードのみが、未知の転写産物がエキソンであることを示唆していることに気付きました(横図)。今回の発見は、研究室のメンバーと実際のデータを前にして議論を尽くしたことにより見つけることができました。(宮脇慎吾)
特記事項
本研究成果は、2020年10月2日(金)に米国科学誌「Science」(オンライン)に掲載されました。
なお、本研究は、日本学術振興会 科学研究費補助金、日本学術振興会 科学研究費助成事業 新学術領域研究「性スペクトラム:領域代表 立花誠」の一環として行われ、クイーンズランド大学 ピーター・クープマン教授との国際共同研究により行われました。
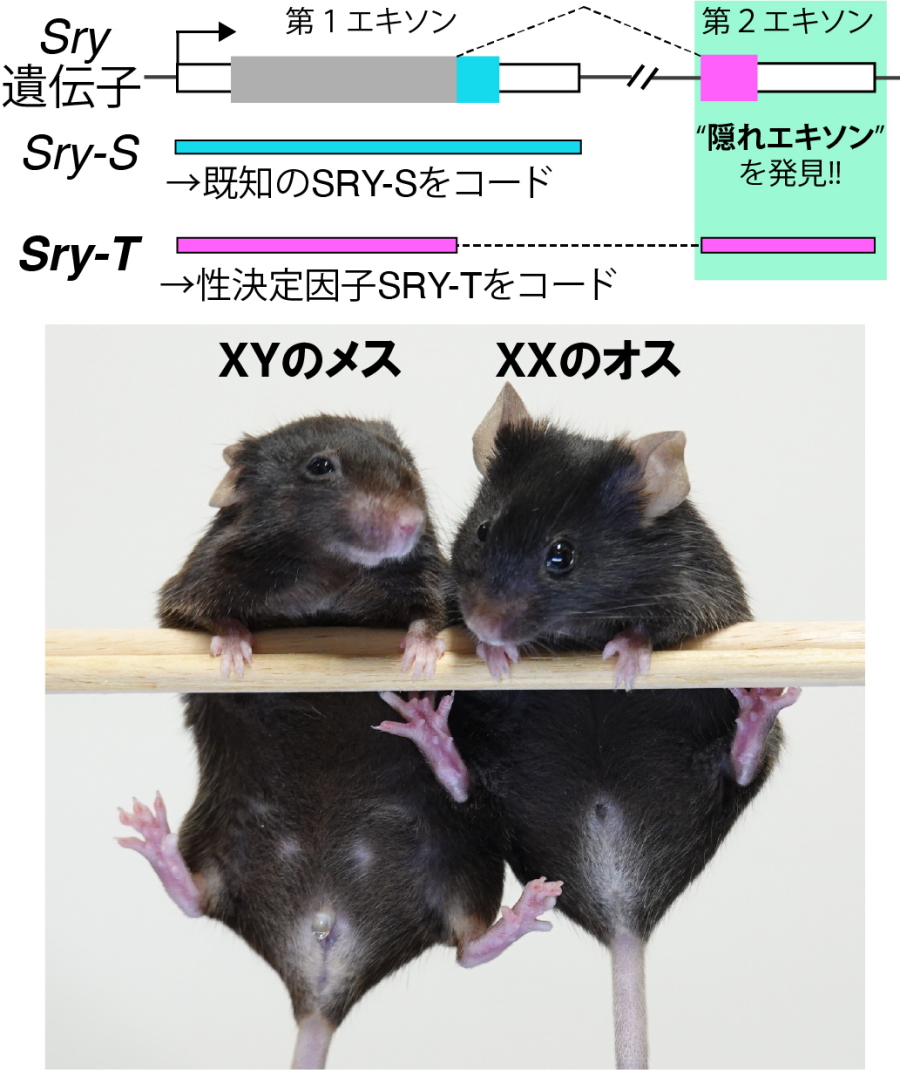
図1
Sry-Tの欠損によりメスに性転換したオス(左)とSry-Tを発現させることによりオスに性転換したメス(右)

図2
(上)重複を許さない解析方法では、転写産物はパリンドローム構造の中に隠れてしまう。一方で重複を許した解析方法により、Sryの近傍に未知の転写産物が認められる。CAGE-seqとlong-read RNA-seqの解析から未知の転写産物はSryのエキソンと判明した。

図3
Sry-Tを欠損すると、オスからメスへ性転換する。Sry-Tを活性化するとメスからオスに性転換する。
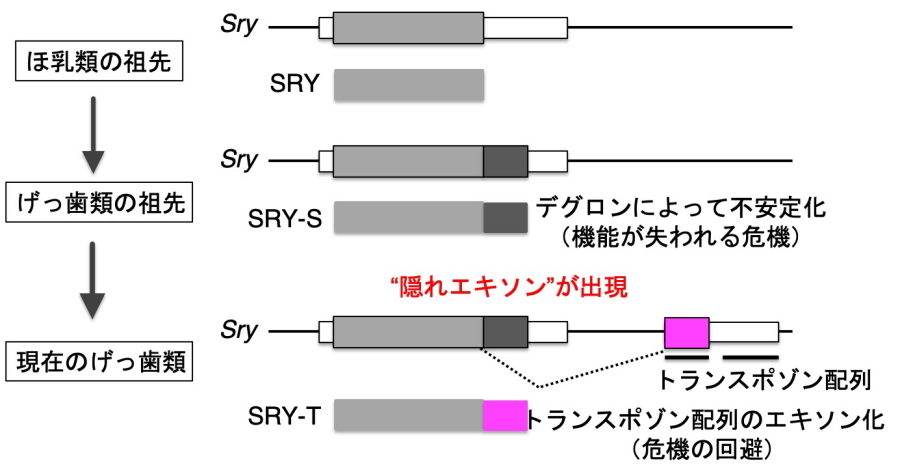
図4
Sry遺伝子の進化
げっ歯類の祖先でSry遺伝子にデグロン配列が出現したと考えられる。今回発見したエキソンはレトロトランスポゾンの配列で構成され、デグロン配列を回避するようにエキソン化が起こったと考えることができる。これにより性決定因子を安定して産生できるようになる。
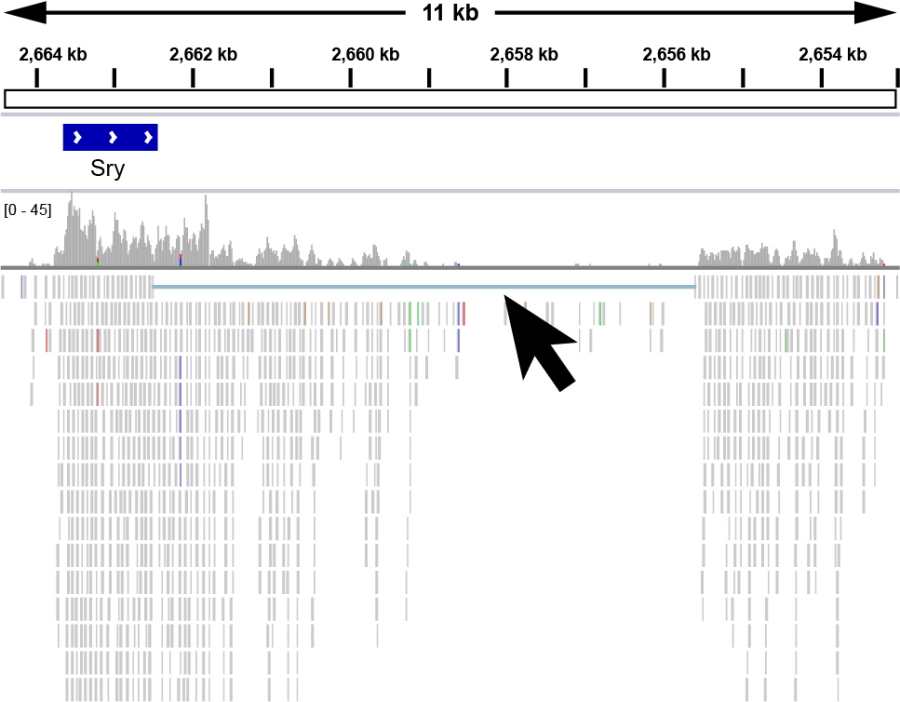
図5
RNA-seqの実験データ。矢印:エキソンを示すリード
用語解説
- エキソン
真核生物の遺伝子では、タンパク質の情報に相当する部分をエキソン(翻訳配列)といい、遺伝情報がコードされていない部分をイントロン(非翻訳、介在配列)と呼ぶ。ゲノム上のエキソンとイントロンはモザイク様で、RNAに転写された後にスプライシングでイントロンが除去されて、残されたエキソンの部分がアミノ酸をコードするメッセンジャーRNAとなる。これまでSryはひとつのエキソンで構成される遺伝子(単一エキソン遺伝子)だと考えられていた。*一般的な表記方法に従い、遺伝子をSry、転写産物をSry-S、Sry-T、タンパク質をSRYと表記した。 - ほ乳類の性決定
ほ乳類は胎仔の時期にはオス、メスのどちらにもなれる能力がある。マウスでは胎性11.5日齢の生殖腺体細胞で一過的にSryが活性化することで、オスになる過程が進行する。実験的に、オス型の性染色体(XY型)を持つ個体でSryを活性化しないとメスになり、メス型の性染色体(XX型)を持つ個体でSryを活性化するとオスに性転換させることができる。 - トランスクリプトーム
ゲノムDNAから転写されたRNA産物(トランスクリプト)を包括的に解析する手法。今回の研究では、RNAシーケンス(RNA-seq)、長鎖RNAシーケンス(long-read RNA-seq)、CAGE-seqを用いて解析した。 - ゲノム編集
CRISPR/Cas9などのシステムを用いて、ゲノムの任意の場所を切断したり、入れ替えたりする技術。今回の論文では、徳島大学の竹本教授らによって開発された、エレクトロポレーションを用いた手法を使用した。 - 性決定遺伝子Sryの発見と歴史的背景
1991年にKoopmanらのグループがSryを含むL741と呼ばれるY染色体のDNA断片をマウスのゲノムに複数コピーを挿入し、Sryを強制的に活性化することでメスからオスへ性転換する実験を実施し、Sryが性決定遺伝子であると示した(P. Koopman., Nature. 1991)。この発見以降30年間、多くの研究がこのL741をもとにして実験されており、オスになるために必要な領域はL741の中にあると考えられていた。しかしながら、近年、このL741をメスのゲノムに単一コピーで挿入しても、オス化することができないことが示され(A. Quinn., PLoS One. 2014)、我々はL741の外側に性決定に不可欠な要素が存在する可能性があると考えた。本研究では、L741の外側にSryの第2のエキソンが存在することを発見した。 - デグロン
タンパクのC末端に特定の配列が存在すると、その配列を認識してタンパク質を積極的に分解するシステムが存在する。この特定の配列がデグロン配列である。デグロン配列を持つタンパク質は速やかに分解される。 - レトロトランスポゾン
ゲノム上に多数存在するレトロウイルス由来の配列。
| 原著論文 | Science 370(6512):121-124 (2020) |
|---|---|
| 論文タイトル | The mouse Sry locus harbors a cryptic exon that is essential for male sex determination |
| 著者 | Shingo Miyawaki (1, 2), Shunsuke Kuroki (1, 2), Ryo Maeda (1, 2), Naoki Okashita (1, 2), Peter Koopman (3), Makoto Tachibana (1, 2)
|
| PubMed | 33004521 |
