プロトカドヘリンγC4が神経細胞死と小脳回路形成を制御することを解明
神経発達障害の病態理解に新たな手がかり
| 原著論文 | Communications Biology 9 (1), Article number: 546 |
|---|---|
| 論文タイトル | Protocadherin γC4 regulates neuronal survival and dendritic self-avoidance |
概要
大阪学大学院生命機能研究科の樋口流音助教、八木健教授らの研究グループは、生理学研究所生体機能調節研究領域の小林俊寛教授、三宝誠技術職員、平林真澄特別協力研究員、北海道大学大学院医学研究院の渡辺雅彦教授、群馬大学医学系研究科の平井宏和教授、今野歩講師、岩手医科大学医歯薬総合研究所の吉岡芳親客員教授、湘南医療大学臨床医学研究所の平林敬浩研究員、奈良県立医科大学医学研究支援センターの金子涼輔准教授らの研究グループとの共同研究として、細胞間接着タンパク質であるプロトカドヘリンγC4(γC4)が出生後の脳発達と小脳回路形成を担う分子であり、γC4が神経細胞の生存と樹状突起の自己回避に不可欠であることを、ゲノム編集マウスを用いた解析により世界で初めて明らかにしました。
γC4は50種類以上のクラスター型プロトカドヘリン遺伝子群(cPcdh)に含まれる1アイソフォームです。これまで、ヒトPCDHGC4の変異が神経発達症候群の原因となることが報告されていた一方で、γC4を欠損させたマウスは新生仔期に致死となるため、出生後の脳発達や神経回路、行動異常がどのように生じるのか、またPcdh-γ遺伝子群の中でγC4が担うアイソフォーム特異的な役割は十分に解明されていませんでした。
今回、研究グループはDOMINO法(図1)により、γC4のみを機能低下させた変異マウスと、γC4のみを完全長で残すマウスを作出し比較解析することで、γC4機能低下で歩行異常やけいれん、胎生期の神経細胞死の増加、小脳プルキンエ細胞の樹状突起自己回避の破綻が生じることを見出しました。さらに出生後にアデノ随伴ウイルス(AAV)でγC4を補うことで自己回避異常が部分的に改善できることを示しました。これにより、γC4を起点とした神経発達障害の分子メカニズム解明を進めるとともに、将来的な治療戦略を検討するための基盤構築につながることが期待されます。
研究の背景
神経発達障害(Neurodevelopmental disorders; NDDs)は、認知・社会性・行動の発達に困難をきたす幅広い疾患群で、近年の大規模ゲノム解析により多くのリスク遺伝子が同定されています。一方で、遺伝子変異が脳発達のどの過程をどのように乱し、症状につながるのかを理解するには、生体(in vivo)で機能を検証できるモデルが不可欠で、遺伝学的変化を、脳回路形成や病態メカニズムの理解と治療へつなげるための実験基盤が求められています。
その候補遺伝子の一つが、細胞膜上でニューロン同士の認識・結合を担うクラスター型プロトカドヘリンファミリーに属するプロトカドヘリンγC4(γC4)です。クラスター型プロトカドヘリンは、シナプス形成や神経回路形成に関わる多様な細胞表面分子として知られ、細胞外カドへリンドメインによる細胞間相互作用に加え、細胞内ドメインがさまざまなシグナル経路を介して樹状突起形成や細胞骨格制御にも関与すると考えられています。実際に、γC4はマウスにおいて神経細胞と個体の生存に必須であることが示され、さらにヒトPCDHGC4の両アレル変異が新規の神経発達症候群の原因となることが報告されています。
しかし、γC4を欠損させたマウスは新生仔期に致死となるため、出生後の脳発達・神経回路・行動への影響を生体レベルで追跡することが難しく、その役割は十分に解明されていません。そこで本研究では、γC4を選択的に改変できる新しいゲノム編集戦略(DOMINO法)を樹立し、γC4機能低下が脳発達や神経回路形成に及ぼす影響を解析できるマウスモデルを構築しました。このモデルにより、ヒト遺伝学で見つかった変異と、脳発達の異常や疾患関連表現型とのつながりを、分子から個体レベルまで連続的に検証できる基盤の確立を目指しました。
本研究の成果
研究グループは、プロトカドヘリンγクラスターの22アイソフォームの中で、γC4が担う役割を検証するために、新しいゲノム編集戦略「DOMINO(DOuble Mutation INducing Open reading frame switch)」法を開発しました(図1)。この方法により、γC4だけを機能低下させた系統(γC4nmd)と、22アイソフォームのうちγC4だけを完全長タンパク質として残す系統(γC4fl-only)を作り分け、γC4の機能を必要かつ十分に評価できる実験基盤を確立しました。
研究グループはまず、γC4nmdマウスの生後表現型を解析し、歩行パターン(足跡解析)に異常が生じることを見出しました(図2)。γC4nmdでは歩幅が短くなるなど運動協調性の低下を示し、加えて転倒やけいれん発作といった異常行動も観察されました。一方で、γC4fl-onlyマウスは外見や行動が野生型とほぼ同等で、γC4タンパク質を完全長で発現することが生後の安定した生存と運動機能に十分であることが示されました。これらの結果は、γC4の細胞内共通領域(γCR)を含む完全長構造が、発達期の脳機能維持に重要である可能性を示します。
次に研究グループは、発生期脳における神経細胞生存への影響を調べるため、胎生18.5日の脳で活性化カスパーゼ3の免疫染色によるアポトーシス(神経細胞死)を解析しました(図3)。その結果、γC4nmd脳では脳幹を中心とした領域で神経細胞死が増加しており、γC4機能低下が発生期の神経細胞生存に影響することが示されました。一方、γC4fl-only脳では神経細胞死は野生型と同程度で異常がなく、γC4タンパク質が完全長で存在することが神経細胞の生存に十分であることが明確になりました。
さらに研究グループは、小脳プルキンエ細胞の樹状突起形態に着目し、神経回路形成に重要な「自己回避(self-avoidance)」を定量評価しました(図4)。γC4nmdマウスでは、樹状突起が本来避けるべき自分自身と交差する頻度が増え、樹状突起の配置が乱れることが分かりました。対照的に、γC4fl-onlyマウスでは自己交差は正常範囲に保たれており、プルキンエ細胞の自己回避にはγC4の完全長発現が必要であることが示されました。これは、運動障害と関連が深い小脳回路の異常が、γC4機能低下により生じうることを示す結果です。
最後に研究グループは、「出生後にγC4機能を補えば細胞異常を改善できるか」を検証するため、アデノ随伴ウイルス(AAV)を用いてプルキンエ細胞へγC4を生後に過剰発現させる回復実験をおこないました(図5)。その結果、γC4を出生後1日齢で導入することで、樹状突起の自己交差が減少し、自己回避の異常が部分的に回復することが分かりました。ただし完全な正常化には至らず、発生期あるいは発達期の適切なタイミングでのγC4の発現と機能維持が重要であることも示唆されました。
研究成果のポイント
- プロトカドヘリンγC4が発達期の神経細胞死の抑制と小脳プルキンエ細胞の樹状突起※1自己回避※2形成に必須であること、さらに出生後のγC4導入で形態異常が部分的に改善し得ることを明らかに。
- ヒトPCDHGC4変異が神経発達障害※3の原因となる一方、既報のγC4欠損マウスは新生仔期に致死となり、出生後の脳発達・神経回路・行動への影響を検証できる実験基盤が不足していた。
- γC4を選択的に改変できる新しいゲノム編集戦略(DOMINO法)の樹立により、新規マウスモデルを確立することで解析が可能に。
- 神経発達障害の病態メカニズム解明を加速するとともに、γC4機能の補完による治療戦略の検討や、プロトカドヘリン機能異常が関与する自閉スペクトラム症・統合失調症など関連疾患研究への応用へつながることに期待。
本研究成果が社会に与える影響(本研究成果の意義)
本研究は、ヒトPCDHGC4(γC4)変異が関与する神経発達障害について、出生後の脳発達段階で何が起きているのかを検証できる実験モデルを提供しました。遺伝子変異の発見だけでは説明できない病態の実体である神経細胞死や神経回路の形成異常を、解剖学・細胞生物学・行動解析を通じて統合的に評価できるようになります。
さらに本研究は、γC4が神経細胞死の抑制や樹状突起の自己回避形成に関わること、そして出生後にγC4を導入することで細胞形態の異常が部分的に改善し得ることを示しました。これらの知見は、発達期の病態メカニズム解明に加え、将来的な治療戦略を検討するための基盤となることが期待されます。また、プロトカドヘリン機能異常が関与すると考えられている自閉スペクトラム症や統合失調症など、関連する神経疾患研究への応用可能性も示します。
研究者のコメント
これまで、ヒト神経発達障害に関わるプロトカドヘリンγC4が神経細胞死の回避に関与していることが明らかになっていました。今回、私たちが樹立したγC4機能低下マウスは成体まで生き残り、ヒト神経発達障害モデルとして解析できました。その結果、驚いたことに小脳プルキンエ細胞における樹状突起異常が発見され、これまでのプロトカドヘリン自己回避モデルでは説明できない新たな分子メカニズムの存在が明らかになりました。 (八木 健)
特記事項
本研究成果は、国際学術誌『Communications Biology』(オンライン)に、2026年3月7日にオンラインで早期公開(編集前の暫定版)されており、最終版は出版社による編集・校正後に公開されます。
なお、本研究は、科研費「学術変革領域研究(A)適応回路センサス」22H05498、24H01221、24H01237、科研費「学術変革領域研究(A)動的コネクトームからの脳機能創発」25H02501、科研費「科学研究費補助金(A)」23H00390(TY)、科研費「科学研究費補助金(C)」24500375、15K06696、22K06457、22K06454、科研費「国際共同研究加速基金(国際共同研究強化)」15KK0331、科研費「新学術領域研究『個体性を生み出す脳のシステムの統合的解明』」17H05937、17H05967、19H04895、19H04922(計画研究および公募研究)、生理学研究所(NIPS)動物資源共同利用研究センターの計画共同研究(Cooperative Study Program:24NIPS303)、日本医療研究開発機構(AMED)の「脳疾患研究のための統合的脳計測技術開発(Brain/MINDS)」JP20dm0207057およびJP21dm0207111ならびに、「Brain/MINDS 2.0(Multidisciplinary Frontier Brain and Neuroscience Discoveries)」JP24wm0625103、また、JST SPRING JPMJSP2138およびJSPS特別研究員奨励費23KJ1447の支援を受けました。

図1 DOMINO法の概略図

図2 γC4nmdマウスでは歩行異常が確認された
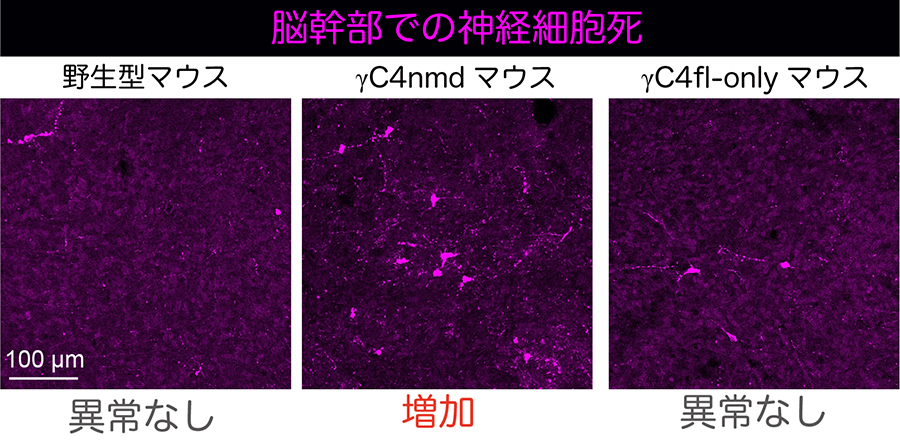
図3 γC4nmdマウスで神経細胞死が増加した
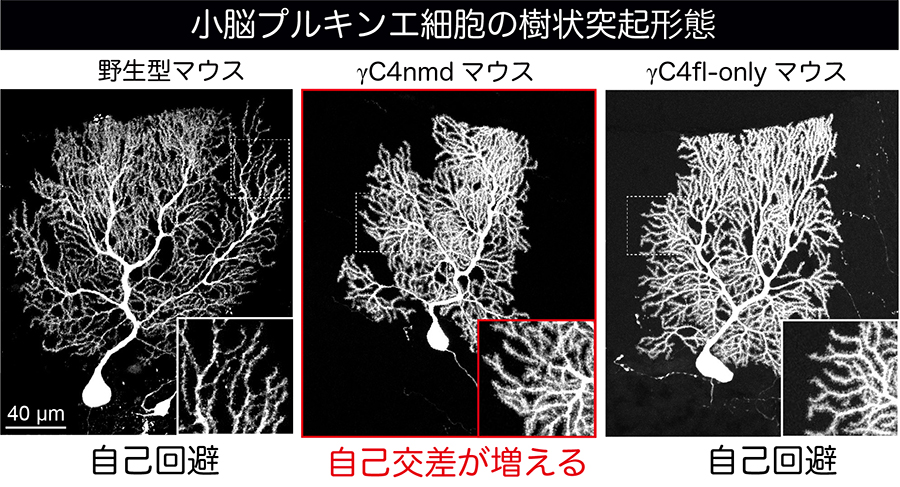
図4 γC4nmdマウスでプルキンエ細胞の樹状突起自己回避が異常になり、自己交差が増えた
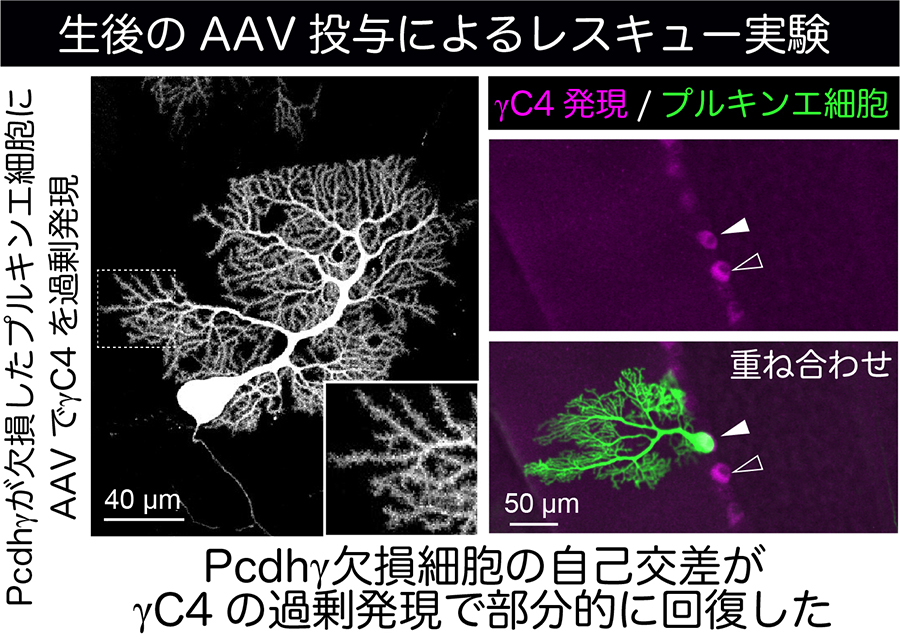
図5 γC4を生後に過剰発現することで、自己交差が部分的に回復した
用語解説
- 樹状突起
神経細胞の細胞体から伸び、他の神経細胞からの入力を受け取る突起。発達期に樹状突起が適切に伸長・分岐し、互いに重なり過ぎないように配置されることで、正常な神経回路が形成される。本研究では大型の神経細胞である小脳プルキンエ細胞の樹状突起に着目した。 - 自己回避
同一ニューロンの樹状突起同士が互いを認識して反発し、自己交差(自分の枝同士の交差)を抑える発達上の仕組み。小脳プルキンエ細胞では、自己回避が樹状突起の整った配置と神経回路形成に重要である。 - クラスター型プロトカドヘリン遺伝子群(cPcdh)
神経細胞の表面に発現する多様化した細胞接着タンパク質群。ゲノム構造としては、多数のアイソフォームがタンデムに並びクラスター構造を形成しており、マウスやヒトでは、Pcdh-α、Pcdh-β、Pcdh-γの3つのクラスターを持つ。cPcdhはアイソフォームごとに独立したプロモーターによって発現制御されており、1つの神経細胞において15種類ほどがランダムに発現することで、神経細胞に個性を与えると考えられている。また、cPcdhは細胞外ドメインによる細胞間相互作用だけでなく、細胞内側の共通領域(constant region)を介して細胞内シグナルにも影響し、樹状突起形態や細胞骨格、神経細胞の生存などに関わりうる。さらに近年は、cPcdh遺伝子群の変異が神経発達障害や精神神経疾患に関連する報告もあり、遺伝学的知見と病態メカニズムをつなぐ重要分子群として注目されている。 - アデノ随伴ウイルス(AAV)
遺伝子を細胞に届けるために利用される小型のウイルス(ベクター)。研究や遺伝子治療開発で広く用いられている。分裂しない神経細胞にも遺伝子を導入でき、標的とする細胞種や脳領域に応じて投与方法やAAVの種類を選択することが可能である。本研究では、出生後にマウス脳にAAVを用いてγC4を導入し、小脳プルキンエ細胞の形態異常が改善し得るかを検証した。 - 神経発達障害
Neurodevelopmental disorders; NDDs。脳発達の過程で神経細胞の生存や神経回路形成が適切に進まないことで、認知・運動・行動などに影響が生じる疾患群。近年、遺伝学研究により多数のリスク遺伝子が同定されているが、変異が脳内でどのような変化(神経細胞死や回路形成異常など)を引き起こすかを生体内で検証することが重要である。最近、ヒトPCDHGC4の両アレル変異によって、進行性小頭症、けいれん発作、関節異常を伴う新規の神経発達症候群を引き起こすことが報告された。
| 原著論文 | Communications Biology 9 (1), Article number: 546 |
|---|---|
| 論文タイトル | Protocadherin γC4 regulates neuronal survival and dendritic self-avoidance |
| 著者 | Ryuon Higuchi (1), Masaki Tatara (1), Satoko Horino (1), Shota Katori (1), Makoto Sanbo (2), Masumi Hirabayashi (2), Masahiko Watanabe (3), Ayumu Konno (4, 5), Hirokazu Hirai (4, 5), Yoshichika Yoshioka (6), Takahiro Hirabayashi (7), Toshihiro Kobayashi (2), Ryosuke Kaneko (1, 8), and Takeshi Yagi (1)
|
| PubMed | 41794998 |
