卵を作る生殖細胞を「死」から守る2重の安全装置を発見
“転写抑制因子 Stand still” と“閉じたクロマチン状態”による抑制
| 原著論文 | PLoS Genetics 22(3):e1012041 |
|---|---|
| 論文タイトル | Transcriptional repression of reaper by Stand still ensures female germline development in Drosophila |
概要
大阪大学大学院生命機能研究科の大学院生の松井将也さん(博士後期課程、研究当時)、甲斐歳惠教授らの研究グループは、ショウジョウバエの卵巣で、卵を作る生殖細胞において「細胞死(アポトーシス)」が過剰に誘導されないよう制御される仕組みの一端をショウジョウバエの卵巣を使って明らかにしました。
私たちの体では、不要・異常な細胞を排除するために「プログラムされた細胞死(アポトーシス)」が働きます。一方で、生殖細胞(卵や精子のもとになる細胞)では、必要な細胞が誤って死んでしまうと繁殖能力に直結するため、細胞死は慎重に抑え込まれる必要があります。
本研究では、ショウジョウバエの雌生殖細胞で、細胞死を引き起こす遺伝子 reaper (rpr) を不用意に働かないようにする因子 stand still (stil) を見いだしました。
stil 遺伝子の機能を失うと、羽化(成虫化)の時点で卵巣の生殖細胞がほぼ消失し、rpr 発現量の増加とアポトーシス(細胞死)に関わる酵素の働きで細胞死が起きることが分かりました。さらに、Stilタンパク質は遺伝子の読み出しを抑えるしくみ(転写抑制)によって rpr の作動を抑えることが分かり、未分化の生殖細胞(生殖幹細胞など)では、「閉じたクロマチン状態」と一致する所見が認められたことから、rpr が読み出されにくい状態であることが示唆されました。
したがって、生殖細胞は (1)Stil による転写抑制と、(2)未分化段階での"読み出されにくさ"という二重の仕組みにより、「死」のスイッチが不用意に入らないよう守られている可能性が示されました(図1)。
今回の研究により、生殖や発生の過程で起こる異常や、細胞死制御の破綻が関わる現象を理解するための基盤知見としての貢献が期待されます。
研究の背景
私たちの体では、不要になった細胞や異常な細胞を取り除くために、プログラムされた細胞死(アポトーシス)が働きます。しかし、生殖細胞(卵や精子のもとになる細胞)にとって、必要な細胞が誤って死んでしまうことは大きな不利益になります。そのため卵巣では、「必要なときには細胞死を起こせる」一方で、「不要なタイミングでは細胞死を確実に抑える」精密な仕組みがあると考えられてきました。
ショウジョウバエでは、細胞死を引き起こす遺伝子群の中でも reaper (rpr) が重要な役割を担いますが、雌の生殖細胞で rpr がどのように“普段は作動しないように”保たれているのかは、十分に分かっていませんでした。さらに、古くから stand still(stil) が雌の生殖細胞の生存に必要であることは知られていたものの、どの遺伝子にどう働きかけているのかといった分子レベルの仕組みは未解明でした。とくに、生殖細胞は未分化な段階(生殖幹細胞など)から分化段階へと連続的に状態が変化するため、段階によって抑えの仕組みが同じかどうかも重要な論点でした。
本研究の成果
本研究ではまず、stil の働きを失ったショウジョウバエの卵巣を詳しく調べ、成虫になる時点で生殖細胞が著しく減少し、卵巣が十分に発達しないことを確認しました(図2)。次に、その原因を検証したところ、生殖細胞でアポトーシスの指標が増えること、そしてアポトーシスを抑える因子を導入すると生殖細胞の消失が大きく抑えられることが分かりました。
さらに解析を進めると、stil の欠損によって reaper(rpr)の発現が増えることが示されました。そこで rpr の制御領域を用いた解析を行い、Stilタンパク質が rpr の転写(遺伝子の読み出し)を抑える方向に働くこと、そしてこの抑制には StilのDNA結合モチーフを含む領域が重要であることを示しました。
一方で、生殖細胞の中でも未分化な段階(生殖幹細胞など)では、rpr の領域が読み出されにくい状態にあることが示唆され(図3)、その背景として、抑制的なクロマチン状態を示す特徴(例:H3K9me3 など)と一致する所見が認められました。 これらの結果から、rpr の誤作動を防ぐ仕組みとして、生殖細胞の幅広い段階で働く「Stilによる転写抑制」に加え、未分化段階では「rprが読み出されにくい状態」が重なって働くという二重の安全装置が存在することを示しました。
研究成果のポイント
- 雌生殖細胞で、細胞死遺伝子 reaper (rpr) が不必要に作動しないように stand still (stil) がrpr の転写を抑制することを発見。
- 卵巣ではアポトーシスが発生段階に応じて厳密に制御されるが、雌生殖細胞で細胞死遺伝子 rpr がどのように抑制されるかは十分に分かっていなかった。
- stil による抑えが生殖細胞の幅広い段階で働くことに加え、未分化な段階(生殖幹細胞など)では、rpr が転写されにくい状態(=閉じたクロマチン状態)が重なる「二重の安全装置」モデルであることが明らかに。
- 細胞死の“起動しやすさ”が生殖細胞の発生段階に応じて調整されるという見方が提示され、細胞死制御の破綻が関わる現象を理解するための基盤知見となることに期待。
本研究成果が社会に与える影響(本研究成果の意義)
生殖細胞の数と質は、個体が次世代を残せるかどうかに直結するため、発生や生殖の過程では細胞死の制御が特に重要です。本研究は、雌生殖細胞でアポトーシス誘導遺伝子 reaper (rpr)が不用意に作動しないよう、「stil による転写抑制」を基本の抑えとして、未分化段階では「rpr が読み出されにくい状態」が重なって働くという、二重の安全装置モデルを示しました。
この二層の組み合わせにより、細胞死の“起動しやすさ”が段階に応じて調整されるという見方を提示し、生殖や発生の過程で起こる異常や、細胞死制御の破綻が関わる現象を理解するための基盤知見としての貢献が期待されます。
特記事項
本研究成果は、米国科学誌「PLoS Genetics」(オンライン)に、3月6日(金)4時(日本時間)に掲載されました。
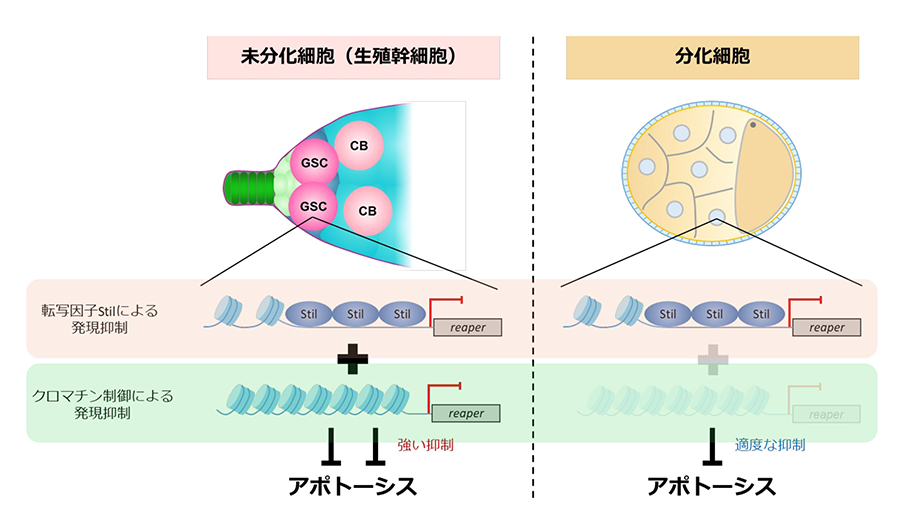
図1 ショウジョウバエの雌生殖細胞のアポトーシス(細胞死)抑制機構
ショウジョウバエのアポトーシス促進因子 rpr は、生殖細胞特異的転写抑制因子 Stand still と閉じたクロマチン状態によって発現が抑えられ、その結果アポトーシスが抑制されることで生殖細胞を維持することを明らかにした。
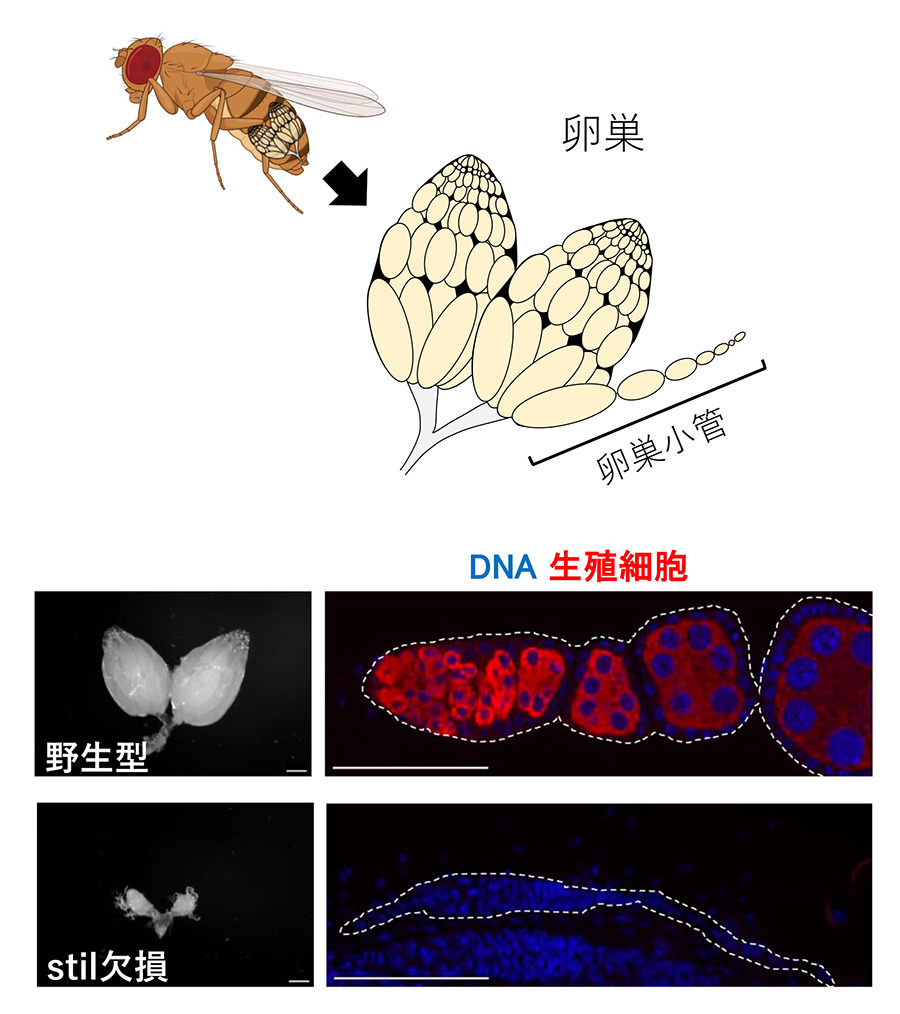
図2 stil 欠損による生殖細胞の消失
ショウジョウバエは卵巣を2つもち、各卵巣15-20本の卵巣管で構成される。各卵巣管内で生殖細胞が分化・成熟し、最終的に卵となる。stil 欠損では、卵巣管内の生殖細胞がほぼ完全に消失する。
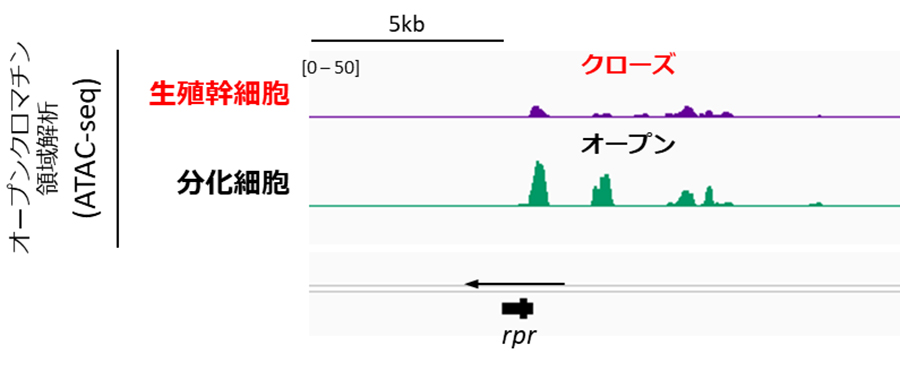
図3 生殖幹細胞と分化細胞のクロマチン構造
生殖幹細胞と分化細胞でクロマチン構造の比較を行った。生殖幹細胞特異的にrpr周辺のシグナルが低く、閉じたクロマチン構造になっていることが示唆された。
用語解説
- 生殖細胞
卵や精子のもとになる細胞。種の存続のために次世代へ遺伝情報を受け継ぐ役割を担い、体細胞とは異なる特別な制御機構のもとで維持・分化され、厳密な品質管理機構によって保たれている。 - アポトーシス
発生や組織の恒常性を保つため、細胞が自ら死ぬ仕組みで、不要になった細胞や異常な細胞を取り除く働きを担う。アポトーシスの制御異常は、癌や神経変性疾患などの様々な病気の原因となる。 - reaper (rpr)
ショウジョウバエにおいてアポトーシスを引き起こす代表的な因子。細胞内でアポトーシス抑制因子の働きを阻害することで細胞死のスイッチを入れる役割を担い、その強い作用から、発生過程やストレス応答において厳密に制御されている。 - stand still (stil)
ショウジョウバエの雌雄の生殖細胞に発現する遺伝子。stil を欠損すると、雌では生殖細胞が消失する。本研究により、Stil は転写抑制因子として、アポトーシスを引き起こす reaper (rpr) の発現を抑え、生殖細胞が死なないよう制御していることが明らかになった。
| 原著論文 | PLoS Genetics 22(3):e1012041 |
|---|---|
| 論文タイトル | Transcriptional repression of reaper by Stand still ensures female germline development in Drosophila |
| 著者 | Masaya Matsui (1), Shinichi Kawaguchi (1), Toshie Kai (1, 2)
|
| PubMed | 41785206 |
