記憶関連分子CREBが脳の神経回路を活性化する仕組みを解明
遺伝子発現の1分子イメージングによる学習・記憶研究の新展開
| 原著論文 | Cell Reports (2023) |
|---|---|
| 論文タイトル | Repetitive CREB-DNA interactions at gene loci predetermined by CBP induce activity-dependent gene expression in human cortical neurons |
概要
大阪大学大学院生命機能研究科の大学院生の渥美友梨さん(博士課程)、菅生紀之特任准教授(常勤)、深圳湾実験室・神経疾病研究所(中国)の山本亘彦客員教授の研究グループは、ヒト神経細胞の核内で学習や記憶に繋がるタンパク質とゲノムDNAの動的振舞いを1分子レベルで明らかにしました。
これまで学習・記憶に転写調節因子CREBと、一緒に働くことが知られ神経疾患の原因遺伝子である共活性化因子CBPが重要であることが知られていましたが、どのような動的な振る舞いが必要とされるのかは不明でした。
今回、1分子イメージング法を利用することで、刺激に応答してCREBが記憶や学習に関連する遺伝子に素早く繰り返し結合することで遺伝子発現を促進することを明らかにしました。また、これにはエピジェネティックな制御を担うCBPによる事前の準備が必要であることを解明しました。これにより、学習・記憶を引き起こす仕組みのより詳細な理解につながるだけでなく、精神神経疾患の発症機構解明にも一石を投ずる成果として期待されます。
研究の背景
脳の神経細胞が刺激を受け取ると、数百種類もの遺伝子が活性化することによって、神経回路の形成・再編が誘導されます。この過程の異常は自閉症、統合失調症といった精神神経疾患とも関連しており、その仕組みを明らかにすることは疾患の病態理解において重要な課題となっています。CREBは、神経細胞の生存、分化、シナプス可塑性などに必要とされるタンパク質で、刺激が入るとCREBが特定のDNA配列と結合することで学習・記憶に関連した遺伝子発現を促進します。さらに、CBPと複合体を形成することによって、RNAポリメラーゼII(RNAPII)をリクルートして遺伝子発現を引き起こします。また、CBPはヒストンアセチル化酵素でもあり、エピジェネティックな制御を担うと考えられています。これまで、生化学的手法を用いてCREBの活性化経路や標的遺伝子が調べられてきましたが、遺伝子発現を促進するための時空間的な分子動態については知られていませんでした。また、これら分子メカニズムの研究は主としてげっ歯類を用いて実施されてきたため、病態理解に向けては、ヒト神経細胞を用いた研究は急務です。
本研究の成果
これらの課題を克服するため、本研究グループはVIB-KU(ベルギー)のPierre Vanderhaeghen教授、岩田亮平研究員のグループと協力してヒトES細胞から分化させた大脳皮質神経細胞の培養系を確立し(図1左上)、核の一部分のみを照らす斜光照明顕微鏡を用いて蛍光標識したCREBとCBPを1分子レベルで可視化して時空間的な動態を入念に解析しました。さらに、東京工業大学の木村宏教授のグループと協力して、CREBとRNAPIIの同時イメージングに挑戦しました。その結果、(1)神経活動が起こる前から神経細胞の核ではCBPによってヒストンアセチル化された微小領域が点在しており、そこには神経活動が起こったときに素早く遺伝子発現できるように学習・記憶関連遺伝子が準備される(図1左下)。(2)刺激が入るとホットスポットとして、CREBはCBPと共にその遺伝子のDNA配列に選択的に数秒程度の結合を繰り返し(図1右上)、それにより活性化型RNAPIIが集積する(図1右下)ことで遺伝子発現が開始される。この2つのステップが学習・記憶に繋がる分子の振る舞いであることを明らかにしました。
研究成果のポイント
- 学習・記憶に重要な遺伝子発現を促進するCREBとCBPタンパク質の振る舞いをヒト神経細胞で可視化することに成功
- 神経活動が起こると、CBPによって準備された学習・記憶に関連する遺伝子にCREBが繰り返し結合することでその遺伝子発現が促進されることを明らかに
- 学習・記憶が起こる仕組みや精神神経疾患の病態理解に期待
本研究成果が社会に与える影響(本研究成果の意義)
本研究のイメージング手法をiPS細胞技術と組み合わせて、患者さん由来の細胞に応用することで、精神神経疾患の病態のさらなる理解につながることが期待されます。
研究者のコメント
本研究では、ヒト神経細胞が刺激に応じて遺伝子発現を制御する仕組みとして、核内1分子イメージング法によりタンパク質とゲノムDNAが時空間的に会合するホットスポットの形成を直接観察することに成功しました。学習・記憶や精神神経疾患の病態を「分子の動き」として理解が進むことが期待されます。(菅生紀之)
特記事項
本研究成果は、2023年12月21日(木)午前1時(日本時間)に米国科学誌「Cell Reports」(オンライン)に掲載されました。
なお、本研究は、文部科学省科研費新学術領域研究(16H06460「スクラップ&ビルドによる脳機能の動的制御」)、日本学術振興会科研費基盤B(19H03325「神経活動依存的な回路形成を担う遺伝子発現調節のダイナミクス」)、基盤C(17K07109「神経細胞分化における転写動態の1分子イメージング解析」)、科学技術振興機構次世代研究者挑戦的研究プログラム(JPMJSP2138)の支援を受けて行われました。
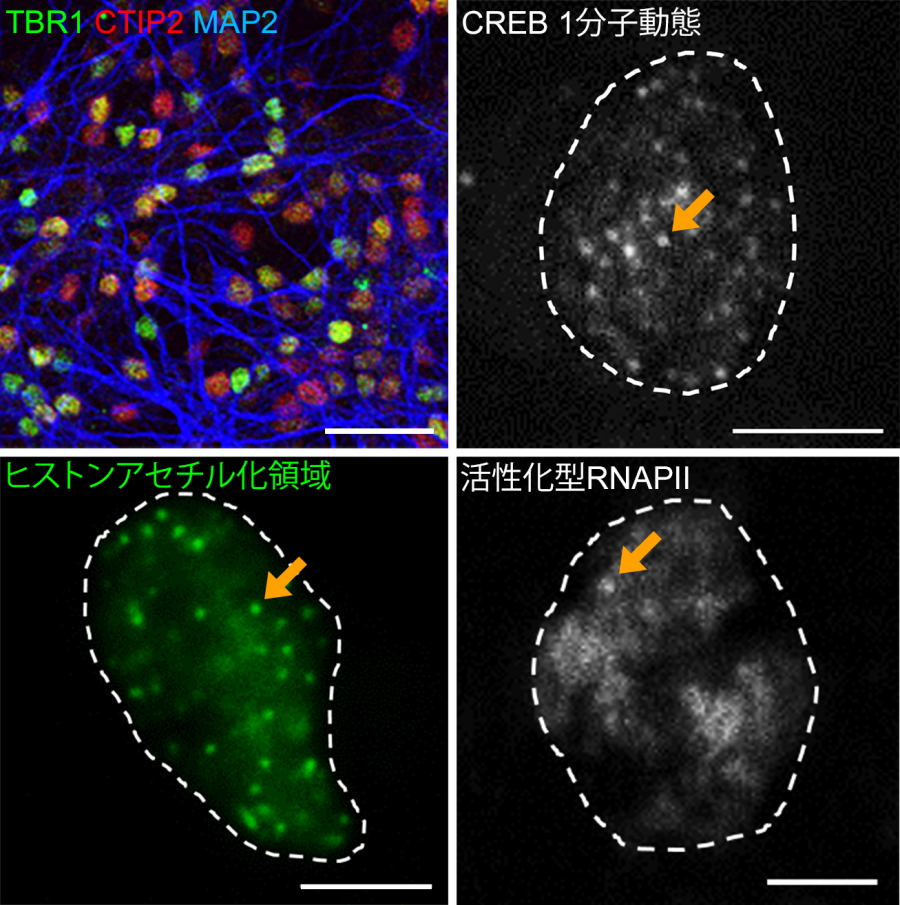
図1.
ヒトES細胞から分化させた大脳皮質神経細胞において(左上)、CREBの1分子動態を解析(右上)。CREBが特定のDNAに繰り返し結合する場所は、高度にアセチル化しており(左下)、そこに活性化型RNAPIIが蓄積することで遺伝子発現を引き起こす(右下)。点線は核の輪郭を表す。スケールバー:50µm(左上)、5µm(その他)。
用語解説
- CREB
サイクリックAMP応答配列結合タンパク質(cAMP response element binding protein)の略で、神経系で重要な転写調節因子の一つ。刺激を受けると、細胞内シグナル伝達によって活性化型に変化して、遺伝子発現を促進する。神経細胞の生存、神経分化、記憶や学習といった様々な場面で重要な働きを担っている。 - CBP
CREB結合タンパク質(CREB binding protein)の略。CREBと結合して、mRNA合成を行うRNAPIIをリクルートすることで、遺伝子発現を促進する。また、ヒストンタンパク質にアセチル基を付加するヒストンアセチル化酵素としても作用する。精神遅延や知的障害を引き起こすRubinstain-Taybi症候群の原因遺伝子として知られている。 - エピジェネティック
細胞がDNA配列を変化させずに遺伝子発現や細胞の機能を変化させる現象のこと。DNAに直接メチル基が付加されるDNAメチル化と、DNAが巻き付いているヒストンタンパク質が様々な修飾を受けるヒストン修飾に大別される。エピジェネティックな修飾がタンパク質とDNAの結合を変化させることで、遺伝子発現を調整する。この変化は環境や経験によって調整され、個体の発達や健康に影響を及ぼすと考えられている。 - RNAPII
RNAポリメラーゼII(RNA polymerase II)の略。DNAを鋳型としてmRNA合成を行う酵素の一つであり、遺伝子発現の初期段階で必須の役割を持つ。RNAPIIが活性化型になることで、mRNA合成の開始、伸長、停止といったプロセスが制御されている。 - ヒストンアセチル化
ヒストン修飾の一つで、アセチル基がヒストンタンパク質に付加されること。これによってDNAとヒストンタンパク質の電気的相互作用が弱まり、DNAに結合しやすい状態になることで、遺伝子発現を促進する。
| 原著論文 | Cell Reports (2023) |
|---|---|
| 論文タイトル | Repetitive CREB-DNA interactions at gene loci predetermined by CBP induce activity-dependent gene expression in human cortical neurons |
| 著者 | Yuri Atsumi (1), Ryohei Iwata (2), Hiroshi Kimura (3), Pierre Vanderhaeghen (2), Nobuhiko Yamamoto (1, 4), Noriyuki Sugo (1, 5)
|
