リソファジーの新規評価系を開発
生活習慣病や認知症予防、老化の抑制に向けた基盤情報のために
| 原著論文 | J. Cell Biol. 222(12):e202204048 (2023) |
|---|---|
| 論文タイトル | The TMEM192-mKeima probe specifically assays lysophagy and reveals its initial steps |
| 研究室サイト | 細胞内膜動態研究室 |
概要
大阪大学大学院医学系研究科の志摩喬之(学振特別研究員、研究当時)(遺伝学)、久万亜紀子特任准教授(常勤)(遺伝学)、吉森保教授(遺伝学/大学院生命機能研究科細胞内膜動態研究室)のグループは、オートファジーによるリソソームの選択的な分解(リソファジー活性)をモニターする新たな評価系を開発しました。
多数の分解酵素を持っているリソソームは、細胞内外の物質の分解を担う酸性オルガネラです。リソソームの膜は様々な因子(シリカ、尿酸結晶など)によって損傷を受けることが報告されていますが、リソソームの内容物が細胞質に放出されることは、炎症、酸化ストレスなどを引き起こし、細胞にとって非常に有害です。リソソームの損傷は神経変性疾患などの病態発症や老化進行とも関わりがあり、近年注目を浴びています。
これまでに研究グループは、損傷を受けたリソソームがオートファジーによって選択的に隔離され分解・除去される現象を発見しました。また最近では、損傷したリソソームがどのようにオートファジーに認識されるのかという仕組みを解明しました。一方、リソファジー以外にも損傷リソソームの修復や生合成に働くリソソーム損傷応答経路が複数報告されました。そのため、これまでに用いていたリソファジーの評価法では、他の損傷応答経路を完全に区別することができないという問題に直面しました。
今回、研究グループは、pHにより励起波長が変化する蛍光タンパク質mKeimaとリソソーム膜タンパク質TMEM192を融合して細胞に発現させることで、リソファジー活性を評価する実験系の開発に成功しました(図1)。また、従来の方法と比較すると、新規評価系ではより特異的にリソファジー活性をモニターすることができることを示しました。さらにこの新規評価系を用いることで、リソファジーの初期段階に機能する因子の同定に成功しました。今後は開発した新規評価系により、リソファジーの分子機構の解明が進むことが期待されます。
研究の背景
リソソームは真核生物の細胞内小器官の一つであり、細胞内外成分の分解を担います。リソソームの中は酸性環境であり、多数の加水分解酵素を有しています。研究グループは、細胞にシリカや尿酸結晶が取り込まれて、リソソームに傷害が生じた際にオートファジーが選択的に損傷リソソームを隔離・修復することを発見し、「リソファジー」と名付けました。リソファジーは腎症の病態悪化を抑制することがわかっており、細胞や個体にとって重要な機能であると考えられています。また近年、リソファジー以外にも複数の経路が損傷リソソームの修復や除去に関わるとの報告が相次ぎました。しかしながら、従来のリソファジー評価系ではこれらの経路を区別して評価することができず、現状、リソファジーに機能する因子の網羅的探索や、その分子機構の解析は技術的に困難でした。
本研究の成果
本研究グループでは、リソファジーを評価するためにTMEM192-mKeimaプローブを開発しました。pHにより励起波長が変化する蛍光タンパク質mKeimaをリソソームに存在する膜タンパク質TMEM192に融合しました。mKeimaは中性環境下(細胞質)では440nmの光で励起されますが、酸性環境(リソソーム)に晒されると586nmに光で励起されるようになります。そのため、リソソーム損傷を誘導する前後のリソソームの蛍光波長の違いを観察することで、リソソーム内に取り込まれたリソソーム(すなわちリソファジー)の検出・可視化が可能となりました(図1)。
このプローブを従来のガレクチン-3アッセイと比較することで、このプローブがよりリソファジーに特異的であることを示し、転写因子TFEBやオートファジーアダプターp62がリソソーム損傷応答には重要であるが、リソファジーには重要ではないことを発見しました。さらに、このプローブを用いることでユビキチン関連因子UBE2L3、UBE2N、TRIM10、TRIM16、TRIM27がリソファジーに重要な因子であることを見出し、TMEM192-mKeimaプローブがリソファジーを調べるための有用なツールであることを示しました。
研究成果のポイント
- 複数のリソソーム損傷応答経路が発見されたが、従来の実験法では各経路を区別して評価することができなかった。
- TMEM192-mKeimaをプローブに用い、リソファジー活性を特異的に評価する実験系を開発した。
- 新規評価系を用いることでリソファジーの分子機構の理解が進むことが予想される。
本研究成果が社会に与える影響(本研究成果の意義)
リソソームの損傷は、動脈硬化の原因となるコレステロールの結晶や、2型糖尿病の原因となるヒトIAPP(膵アミロイドペプチド)、神経変性疾患の原因となるα-シヌクレイン、さらには老化の進行によって起きることが報告されています。また、損傷リソソームを取り除くリソファジーが、高尿酸血症における腎症の病態悪化を抑制することがマウスを用いた実験で示されています。よって、損傷したリソソームを修復してリソソームを正常に保つことが大変重要です。リソファジーを始めとする損傷リソソーム応答の理解は、高齢化社会において問題となる生活習慣病や認知症の予防、あるいは老化の抑制に重要であると考えられます。本研究成果であるリソファジーの活性を特異的に測定することができる新規評価系は、リソファジーの分子機構の解明の突破口になると期待され、さらには、上記の疾患の理解や予防薬/治療薬などの開発に向けた基盤情報を得るために活用できます。
研究者のコメント
リソソーム特異的オートファジー(リソファジー)は、10年前に私たちの研究室が世界に先駆けて発見した現象です。最近、リソファジー以外にも損傷リソソームの修復に働く様々な経路が次々に発見され、リソソームを正常に保つことの重要性が注目されています。リソソーム損傷は老化や生活習慣病の過程で起こりやすいことから、オートファジーの研究がこれらの予防に役立ち、健康長寿の実現に繋がることを期待しています。(久万亜紀子)
特記事項
本研究成果は、国際科学誌「Journal of Cell Biology」に、10月6日(金)に公開されました。
なお、本研究は、革新的先端研究開発支援事業(AMED-CREST)研究開発領域、JST戦略的創造研究推進事業CREST(吉森保)および、日本学術振興会(JSPS)科学研究費助成事業(JP17gm5010001、JP17gm0610005、JP23gm1410014、JPMJCR17H6、JP19K06637、22H04982、2KJ2105)の研究助成により実施されました。
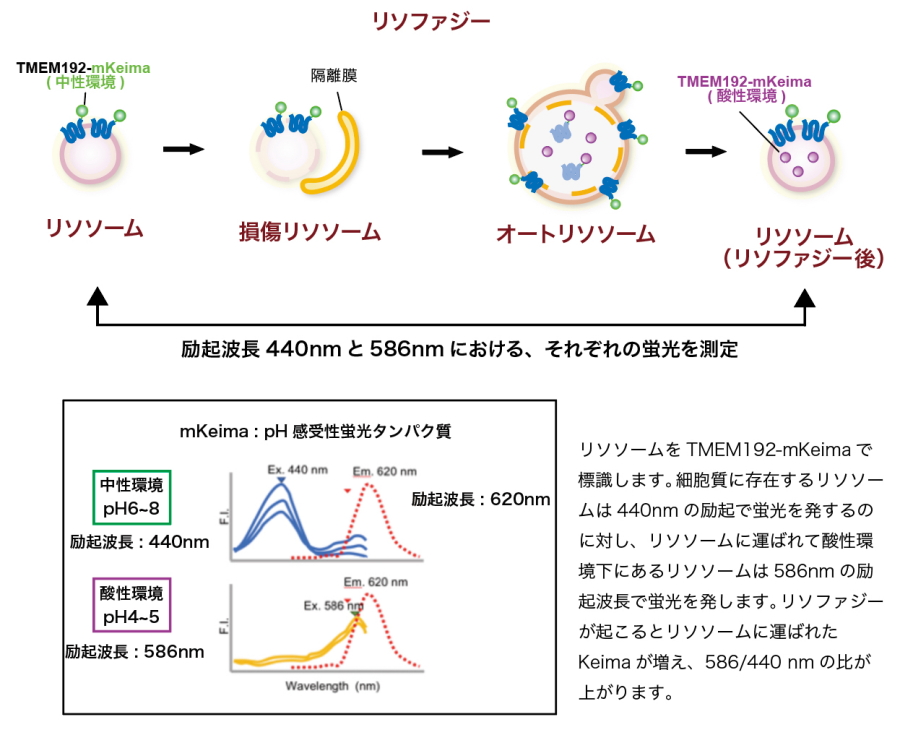
図1.TMEM192-mKeimaを用いた新規リソファジー評価系の模式図
用語解説
- オートファジー
細胞が自己の一部を分解する機能のこと。まず、オートファゴソームと呼ばれる脂質二重膜で隔離され、それがリソソームと融合してオートリソソームを形成後、リソソーム内の加水分解酵素により分解される。オルガネラなどを選択的に分解する選択的オートファジーも存在する。 - リソソーム損傷応答経路
損傷を受けたリソソームに対応するための細胞内の経路の総称であり、近年、損傷膜の修復、新規リソソームの生合成、損傷リソソームの除去、脂質の輸送などの経路が報告されている。 - 蛍光タンパク質mKeima
励起波長がpHにより大きく変化する蛍光タンパク質。中性環境下では励起波長は440nmだが、酸性環境下では586nmにシフトする。この2つの励起波長から得られる蛍光スペクトルを比較することで、mKeimaがどちらの環境にいるかを判断することができる。 - ユビキチン
76個のアミノ酸からなる小さなタンパク質。通常鎖状に連なったユビキチン鎖として分解や輸送、シグナル伝達などの現象に関わる。選択的なオートファジーによる分解の際にはユビキチン鎖が目印となることが報告されている。
| 原著論文 | J. Cell Biol. 222(12):e202204048 (2023) |
|---|---|
| 論文タイトル | The TMEM192-mKeima probe specifically assays lysophagy and reveals its initial steps |
| 著者 | Takayuki Shima (1), Monami Ogura (2), Ruriko Matsuda (2), Shuhei Nakamura (1, 2, 3), Natsuko Jin (1), Tamotsu Yoshimori (1, 2, 4), Akiko Kuma (1)
|
| PubMed | 37801070 |
