副甲状腺ホルモンが骨量を増加するメカニズムを解明!
SLPIという骨形成と骨吸収のバランサーの発見
| 原著論文 | Nat. Commun. (2021) |
|---|---|
| 論文タイトル | SLPI is a critical mediator that controls PTH-induced bone formation |
| 研究室サイト | 免疫細胞生物学研究室〈石井 優 教授〉 |
概要
大阪大学大学院生命機能研究科免疫細胞生物学研究室の森本彬人特任研究員(常勤)、菊田順一准教授、石井優教授(国立研究開発法人医薬基盤・健康・栄養研究所招へいプロジェクトリーダー)らの研究グループは、副甲状腺ホルモン(PTH)による骨量増加のメカニズムを明らかにしました。
生体の骨は、骨を壊す破骨細胞と骨を作る骨芽細胞が協調して働き、骨の再構築(骨リモデリング)を生涯にわたって繰り返すことでその強度を維持しており、様々なホルモンや薬剤によりそのバランスが調節されます。PTHには、骨吸収を促して血中にカルシウムなどのミネラルを供給する他に、骨吸収から骨形成への移行を促して骨を修復する作用があります。しかし、PTHが骨芽細胞と破骨細胞を協調的に制御する分子メカニズムについて、これまでその詳細な機序は明らかにされてきませんでした。
本研究グループは、これまでに独自で開発した生体イメージング技術により、生体内での骨リモデリングの様子を可視化し、PTHが骨芽細胞と破骨細胞の細胞間相互作用を促すことを明らかにしてきました。今回、研究グループはPTH投与後の骨芽細胞の遺伝子発現を網羅的に解析し、骨芽細胞内でSLPIというタンパク質の発現が亢進し、さらにPTHがSLPIを介して骨量を維持していることを発見しました。さらに、SLPIには1.骨芽細胞による骨形成を促す作用、2.破骨細胞を骨芽細胞の近くに引き寄せて骨吸収を抑制する作用、の二つの役割があることを見出しました(図1)。今回の研究成果によって、骨粗しょう症など骨疾患の治療により効果的な治療薬開発の進展につながることが期待されます。
研究の背景
骨の構造と機能は、破骨細胞による骨吸収と骨芽細胞による骨形成を繰り返し、自ら再構築することによって、その強靭さとしなやかさを維持しています。骨吸収と骨形成のバランスが崩れると、骨粗しょう症や骨硬化症などの骨疾患が発症し、骨は脆弱になります。そのため、骨吸収と骨形成のバランスをいかに保つかということは、骨のメンテナンスを考える上で非常に重要です。
PTHは、骨吸収から骨形成への移行(骨カップリング)を促進することで骨量を増やすことが知られており、骨粗しょう症治療薬の要として広く世界で使われています。本研究グループは過去に、生体骨組織イメージング技術を独自に開発し、PTHの薬効評価を行ったことがあります。PTHを投与したマウスでは、薬剤を投与してない群と比較して、骨芽細胞と破骨細胞の細胞間相互作用が増加し、骨吸収を抑制することが分かっています。しかし、PTHがどのように骨吸収と骨形成を同時に制御しているのか、その詳細な分子メカニズムは明らかになっていません。
本研究の成果
本研究グループは、骨芽細胞と破骨細胞の細胞間相互作用に関わる分子メカニズムを検討するために、PTHを連日投与したマウスから骨芽細胞を分離し、次世代シーケンサーを用いた網羅的遺伝子発現解析を行いました。その結果、創傷治癒やタンパク分解酵素に関わる遺伝子の多くがPTHによって発現変動していることを見出し、その中でもセリンプロテアーゼ阻害作用をもつ低分子タンパク質SLPIの発現が最も顕著に増加していることが分かりました。次に、SLPIを欠損したマウスを用いて、SLPIがPTHの骨量増加作用に与える影響を解析したところ、SLPI欠損マウスでは野生型マウスと比較してPTHの骨量増加作用が有意に減少していました(図2)。SLPIが欠損したマウスではPTH投与下で、骨吸収が亢進し、骨形成が減弱していました。このことから、PTHが骨吸収と骨形成のバランスをとる中で、SLPIは骨吸収に傾きすぎないように骨代謝を調節していることが明らかになりました。SLPIを過剰に発現させた骨芽細胞は盛んに細胞分裂を行うほか、Runx2やOsterixという骨芽細胞機能に必須のタンパク質の発現が高いことが分かりました。さらに、SLPIを過剰に発現した骨芽細胞は、破骨細胞との細胞間接着能が高く、細胞間相互作用により骨吸収を抑制することが分かりました。最後に、本研究グループは、独自に開発した生体骨組織イメージング技術を用いて、SLPIを欠損したマウスでの破骨細胞と骨芽細胞の相互作用を解析しました。その結果、PTH投与下において、SLPI欠損マウスでは野生型マウスと比較して、骨芽細胞と破骨細胞の細胞間相互作用の頻度が小さいことが明らかとなりました(図3)。以上の結果から、SLPIは骨芽細胞に直接的に作用して骨形成を促進しているほか、骨芽細胞と破骨細胞の細胞間相互作用を増加することで骨吸収と骨形成の両面を制御していることが明らかになりました。
研究成果のポイント
- 副甲状腺ホルモン(PTH)は体の中の骨やカルシウムを制御する重要なホルモンである。投与のやり方によっては骨量を増加させることが知られており、現在骨粗しょう症の治療薬としても用いられているが、詳細な分子メカニズムはよくわかっていなかった。
- 今回、PTHが骨に作用すると、骨芽細胞が低分子タンパク質であるSLPI(secretory leukocyte protease inhibitor)を発現し、これが骨を作る骨芽細胞の骨形成機能を上げると同時に、細胞外に分泌されて、破骨細胞との相互作用(カップリング)を制御し、骨を壊す破骨細胞による骨吸収(骨破壊)を抑制することを明らかにした。
- 骨形成と骨吸収を協調的に制御する新規分子を発見したことで、骨代謝を調節する新たな骨疾患治療薬への応用が期待される。
本研究成果が社会に与える影響(本研究成果の意義)
骨粗しょう症の治療では、骨吸収を抑える薬剤に比べて骨形成を促進させる薬剤は限られており、骨を再生させる治療薬の開発が望まれています。本研究成果は、骨疾患治療薬薬であるPTH製剤の臨床的意義をさらに高めるとともに、骨粗しょう症など骨疾患の治療により効果的な骨疾患治療薬の開発につながることが期待されます。
特記事項
本研究成果は、2021年4月9日(金)午後6時(日本時間)に英国科学誌「Nature Communications誌」(オンライン)に掲載されました。
本研究成果は、国立医療研究開発機構(AMED)の先端的バイオ創薬等基盤技術開発事業における「生体組織イメージングに基づいたバイオ医薬品の新規評価基盤技術の開発」(研究代表者:石井優教授)の一環として得られました。
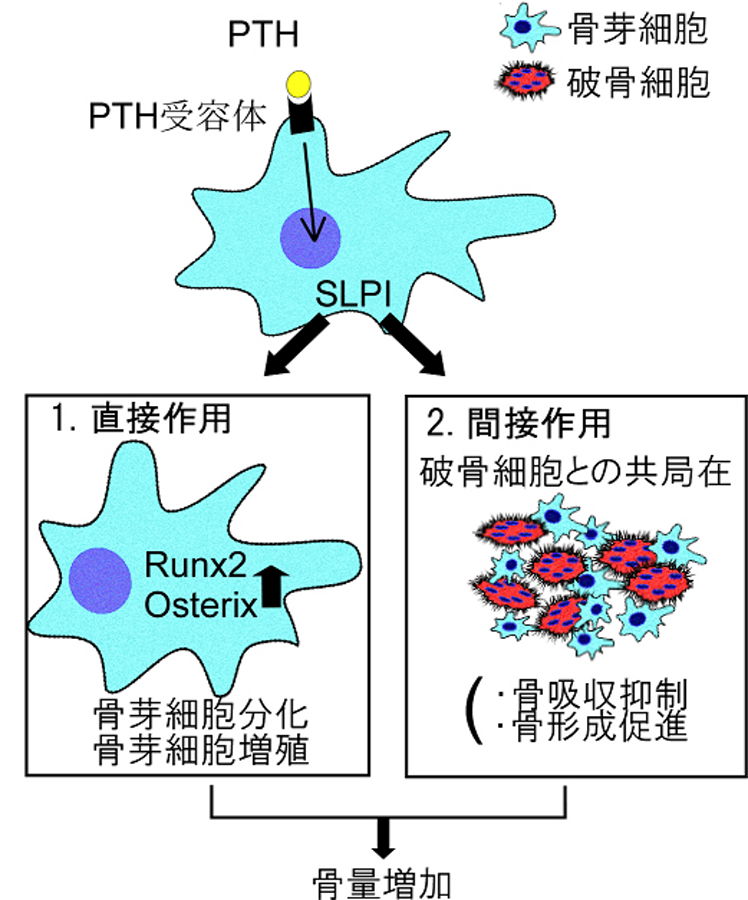
図1.PTHによる骨量増加メカニズム
PTHが骨芽細胞上に発現するPTH受容体に作用するとSLPIが発現するようになる。SLPIは骨芽細胞の分化を直接制御すると同時に、骨芽細胞の周りに破骨細胞を引き寄せることで、骨吸収を抑制する。
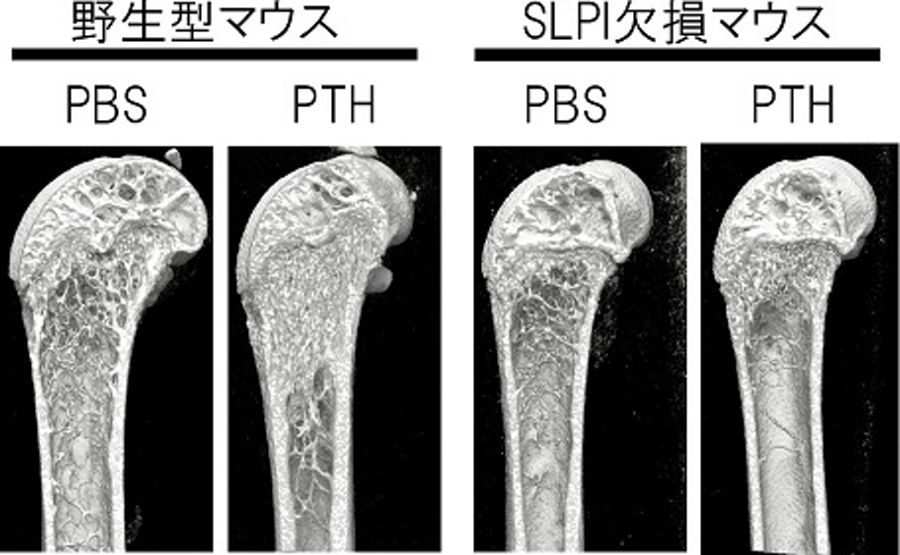
図2.SLPIを欠損すると、PTHの薬効が小さくなる
マウス大腿骨遠位端のµCT解析。野生型マウスではPTH投与により海面骨量が増加するが、SLPI欠損マウスでは、この薬効が有意に小さくなる(P < 0.0001)ことを示す。
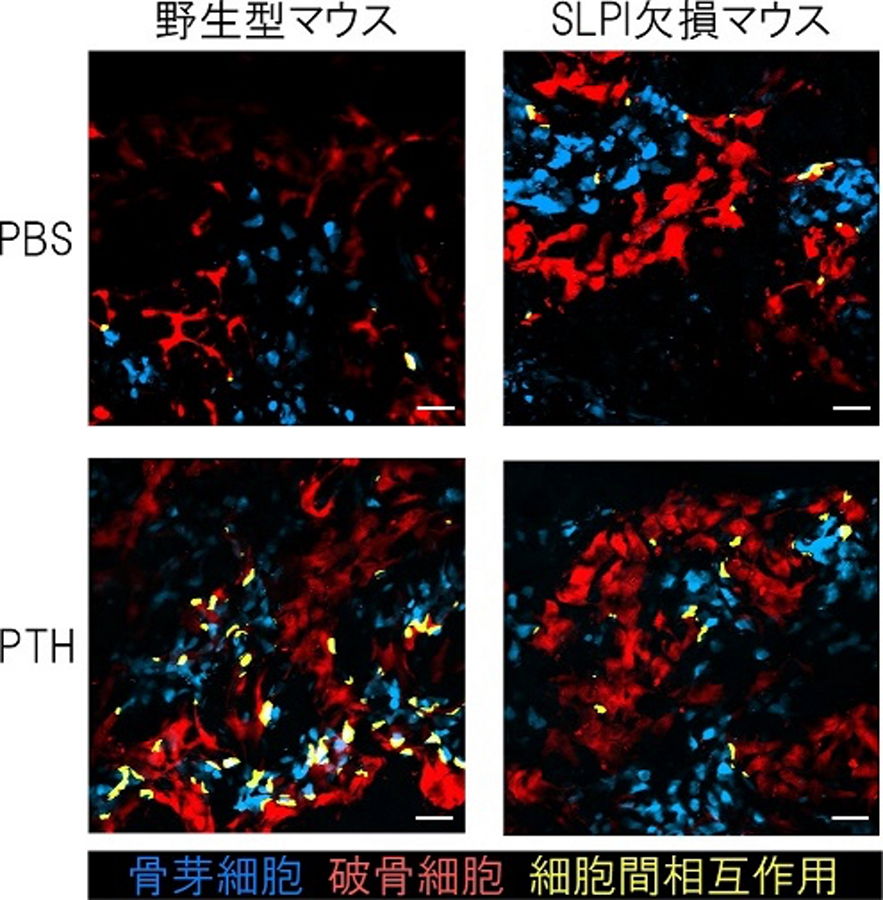
図3.SLPIは骨芽細胞と破骨細胞の相互作用を調節する
マウス頭蓋骨の生体イメージング解析。野生型マウスではPTH投与により黄色で示される破骨細胞と骨芽細胞の細胞間相互作用が増加するが、SLPI欠損マウスでは、この効果が小さくなることを示す。
用語解説
- 副甲状腺ホルモン(PTH)
もともとは骨吸収を促進することで血液中のカルシウム濃度を上げる作用が知られていた。しかしながら、投与方法によっては骨量を増加させることが示され、2010年に、ヒト副甲状腺ホルモン1-34(テリパラチド)が骨粗しょう症治療薬として製造販売承認された。PTH製剤は、骨形成を促進する薬剤として初めて承認された。強力な骨形成作用により、十分な骨量増加が得られ、優れた骨折予防効果が証明されている。 - SLPI(secretory leukocyte protease inhibitor)
組織傷害時に、主に白血球が分泌する代表的なセリンプロテアーゼインヒビター。炎症の後期で発現が上昇し、炎症を抑制するとともに組織再生を誘導することが知られている。近年、骨でも発現していることが報告されていたが、生体骨組織内での作用は分かっていなかった。 - 骨リモデリング
骨の再構築は破骨細胞分化により開始され、破骨細胞により古い骨が溶かされる。その後、骨芽細胞により新しい骨が造られ、溶かされた部分が完全に覆われる。この一連のサイクルが繰り返されることで骨量が維持されている。この骨の再構築を骨リモデリングとよぶ。 - 生体イメージング技術
実験動物を生かしたまま顕微鏡に乗せ、臓器内部の細胞や分子の動きをリアルタイムで解析する手法。特殊な顕微鏡を使用することで、硬い石灰質に囲まれた骨の内側を生きたまま観察し、骨リモデリングを行う細胞の挙動を解析することができる。
| 原著論文 | Nat. Commun. (2021) |
|---|---|
| 論文タイトル | SLPI is a critical mediator that controls PTH-induced bone formation |
| 著者 | Akito Morimoto (1, 2), Junichi Kikuta (1, 2, 3), Keizo Nishikawa (1, 2), Takao Sudo (1, 2), Maki Uenaka (1, 2), Masayuki Furuya (1, 2), Tetsuo Hasegawa (1, 2), Kunihiko Hashimoto (1, 2), Hiroyuki Tsukazaki (1, 2), Shigeto Seno (4), Akira Nakamura (5), Daisuke Okuzaki (2, 6), Fuminori Sugihara (7), Akinori Ninomiya (7), Takeshi Yoshimura (8), Ryoko Takao-Kawabata (9), Hideo Matsuda (4), Masaru Ishii (1, 2, 3)
|
| PubMed | 33837198 |
