神経管形成メカニズムの新規分子機構を明らかに。鍵は「タイトジャンクション」にあった!
上皮形態形成機構解明に光
| 原著論文 | Embo J. e104712 (2020) |
|---|---|
| 論文タイトル | A microtubule-LUZP1 association around tight junction promotes epithelial cell apical constriction |
| 研究室サイト | 生体バリア細胞生物学研究室〈月田 早智子 特任教授〉 |
概要
神経管は上皮細胞シートがアピカル収縮という機構で湾曲し、内腔へと陥入していくことで形成されます。神経管形成異常は無脳症や二分脊髄などの重篤な先天性の神経系奇形の原因として知られています。神経管形成のメカニズムの解明の重要性は言うまでもないですが、その中心的な役割を果たす上皮細胞におけるアピカル収縮の分子メカニズムは十分には解明されていませんでした。
今回、大阪大学大学院医学系研究科の矢野智樹助教、大学院生命機能研究科の月田和人特任研究員(京都大学大学院医学研究科臨床神経学)、田村淳特任准教授(帝京大学医学部准教授)、月田早智子特任教授(帝京大学戦略的イノベーション研究センター教授)らの研究グループは、微小管結合タンパク質LUZP1が細胞の密着結合、タイトジャンクション(TJ)に局在し上皮細胞においてアピカル収縮を制御していることを発見しました(図)。TJに局在するLUZP1がアピカル収縮に重要なアクトミオシンリング(circumferential ring: CR)の収縮について、ミオシン軽鎖の脱リン酸化活性を直接阻害することで、アピカル収縮阻害を起こすという、これまで認識されていなかった新規の分子機構の発見といえます。さらに、その阻害効果が微小管により増強されるという点も新しい所見として注目されます。将来的には神経管形成異常、消化管形成異常など広い病態の治療へ繋がっていくことが期待されます。
研究の背景
上皮細胞は、主にTJと接着結合(アドヘレンスジャンクション; AJ)が共同してAJC(apical junctional complex)として機能することにより、互いに側面で強く接着し、上皮細胞シートを形成します。個体はその発生過程において、2次元的に広がる上皮細胞シートが折り畳まれることで、3次元的な立体構造を構築します。典型的な例のひとつとして、神経管の形成があります。神経管は上皮細胞シートが湾曲し、内腔側に折れ曲がることにより管を作って上皮細胞シートから切り離されることで体腔内に形成されますが、この上皮細胞の湾曲を引き起こす原動力が上皮細胞シートのアピカル収縮による形態変化です。
上皮細胞のアピカル収縮は、脊椎動物においては、AJCに沿ってその細胞質側に形成されたCRが収縮することにより引き起こされます。このCRの収縮にはROCK1(Rho-associated, coiled-coil containing protein kinase 1)によるミオシン軽鎖のリン酸化が必須であることが知られていましたが、今回TJに局在するLUZP1によるミオシン軽鎖の脱リン酸化阻害は全く新しい観点といえます。
本研究の成果
研究グループはTJに微小管が配行する意義に興味をもち、TJに局在する微小管結合タンパク質の探索を行い、微小管結合タンパク質LUZP1を同定しました。そして、培養上皮細胞やマウス上皮組織において、LUZP1がTJに沿ったCRに局在することを見出しました。次に研究グループは、LUZP1遺伝子をノックアウト(KO)した培養上皮細胞を詳細に解析し、LUZP1欠損細胞では、CRのミオシン軽鎖のリン酸化が著しく低下し、それによりアピカル収縮が顕著に阻害されていることを発見しました。さらに、その分子機構を詳細に解析し、LUZP1が、リン酸化ミオシン軽鎖に強く結合して、脱リン酸化酵素の働きを抑えることを見出しました。その働きはLUZP1が微小管に結合することでより増強されました。
これらの結果により、TJに局在するLUZP1は脱リン酸化酵素を阻害することで、CRのミオシン軽鎖の脱リン酸化を防ぐことがわかりました。それにより、ミオシン軽鎖のリン酸化レベルが保たれ、CRの収縮が促進されて、アピカル収縮が引き起こされると考えられます。
LUZP1遺伝子欠損のマウスでは神経管形成異常を引き起こすと報告されており、今回新たに発見されたLUZP1に基づくアピカル収縮の分子機構は、神経管形成異常にとどまらず、消化管形成異常などの更なる病態解明、ひいてはその治療法の開発へと繋がることが期待されます。
研究成果のポイント
- 上皮細胞シートにおいて、上皮細胞のアピカル部(細胞の表面、頭頂付近)が収縮し上皮細胞の形態を変化させる、アピカル収縮は神経管形成等、上皮形態形成に重要である。本研究ではその詳細新規メカニズムを発見した。
- 細胞接着の1つである密着結合(タイトジャンクション;TJ)において微小管結合タンパク質であるLUZP1が、ミオシン脱リン酸化酵素を阻害することで、アピカル収縮を制御していることを見出した。
- アピカル収縮のTJにおけるLUZP1を介した新規分子機構の解明は、神経管形成異常、消化管形成異常などの更なる病態解明、ひいては治療へと繋がることが期待される。
本研究成果が社会に与える影響(本研究成果の意義)
神経管形成異常によって無脳症、脳瘤、二分脊椎など先天性の重篤な神経系奇形が引き起こされますが、詳細な分子メカニズムは十分には明らかになっておらず、治療法も不十分です。今回、神経管形成の中心機構となる上皮細胞アピカル収縮の新規メカニズムの詳細な解明により、将来的には神経管形成異常の治療や消化管形成異常などの治療へと繋がっていくことが期待されます。
研究者のコメント
神経管形成におけるアピカル収縮と細胞間接着との連関の研究には、歴史的に、ショウジョウバエがモデル動物としてよく用いられてきました。しかし、無脊椎動物であるショウジョウバエにはTJがありませんので、TJについてはほとんど注目されていませんでした。今回TJがアピカル収縮の制御に重要であることが示されたことはアピカル収縮と細胞間接着研究にとって新しい展開であると考えています。また、TJに結合する微小管の役割がはじめて明らかになったことも細胞生物学的新規性が高いと思われます。アピカル収縮を引き起こすために、TJでミオシン軽鎖の脱リン酸化酵素が阻害されることは、細胞間バリアを形成するTJにおけるCRの収縮力学制御の観点で非常に興味深いことと思います。この発見が、神経管形成異常や消化管異常などの病態の解明や治療法の開発の一助になることを期待いたします。(矢野智樹助教、月田和人特任研究員)
特記事項
本研究成果は、欧州科学誌「The EMBO journal誌」に2020年12月22日(火)午後8時(日本時間)に公開されました。
なお、本研究成果は、科学技術振興機構(JST)戦略的創造研究推進事業CREST「生命動態の理解と制御のための基盤技術の創出」(研究総括:山本雅 沖縄科学技術大学院大学細胞シグナルユニット 教授)における「細胞間接着・骨格の秩序形成メカニズムの解明と上皮バリア操作技術の開発」(研究代表者:月田早智子 教授)、日本学術振興会(JSPS)科学研究費補助金特別推進「JP19H05468」(研究代表者:月田早智子 教授)、日本学術振興会(JSPS)科学研究費補助金若手研究「JP18K14696」(研究代表者:矢野智樹)、日本学術振興会(JSPS)科学研究費補助金基盤研究B「JP16H05121」(研究代表者:田村淳)の一環として得られました。
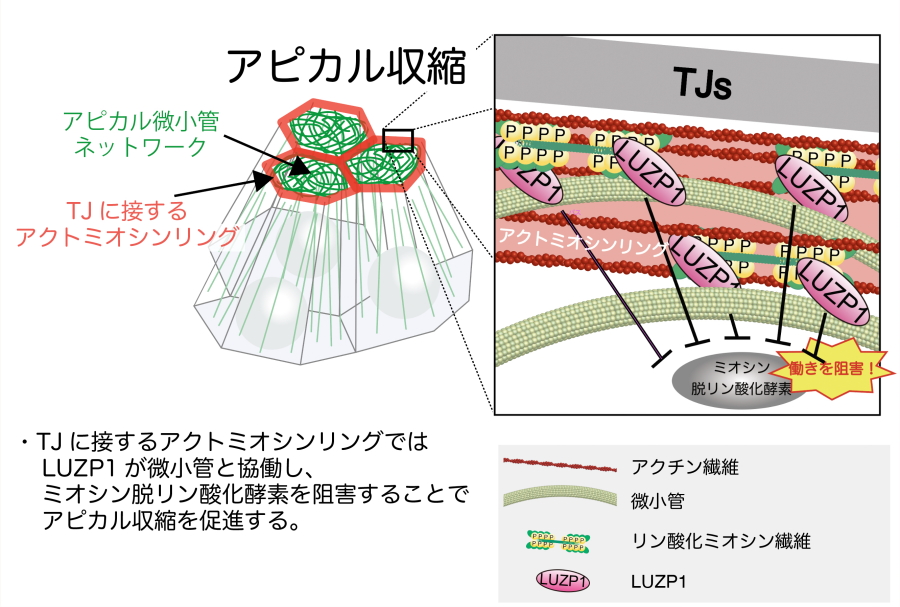
図1.
タイトジャンクションに局在する微小管とLUZP1が協働しアピカル収縮が促進される
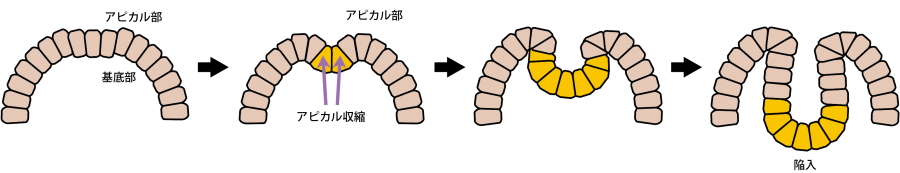
図2.アピカル収縮
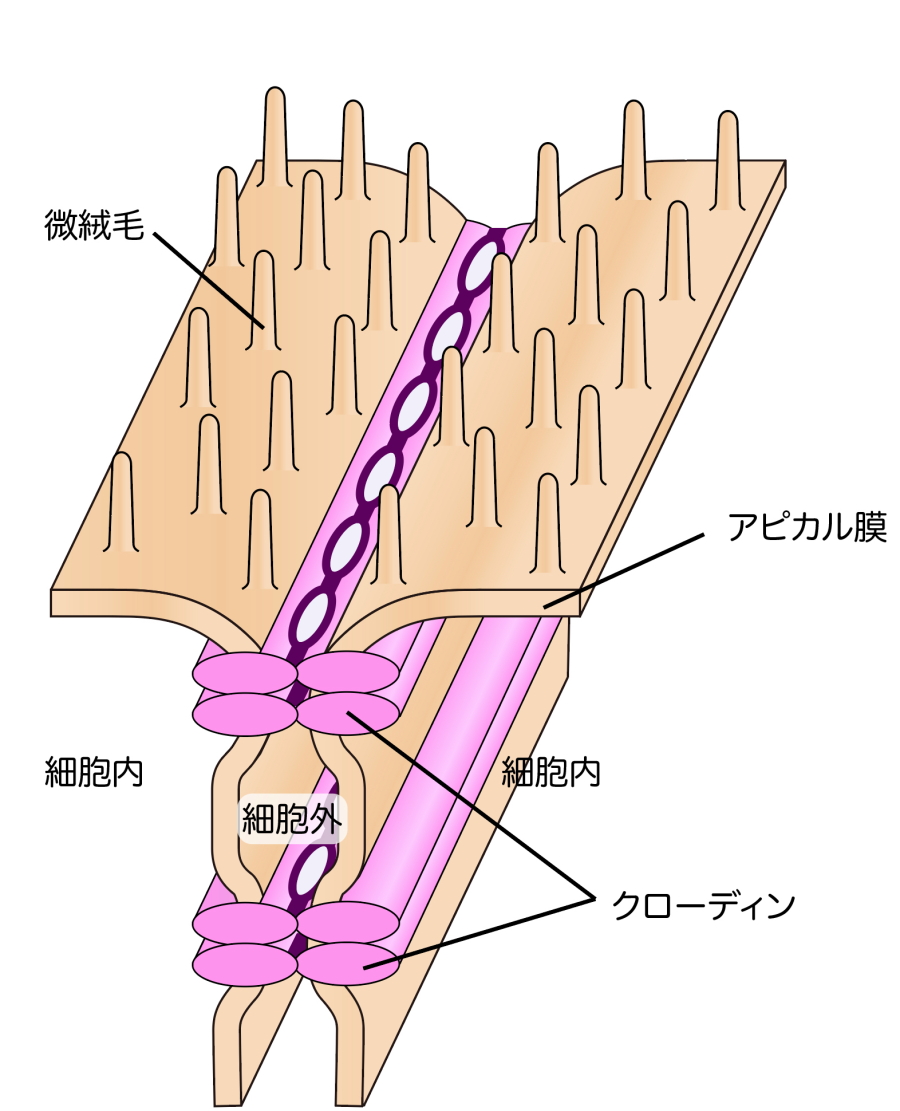
図3.隣り合う上皮細胞間のタイトジャンクション
用語解説
- アピカル収縮
上皮細胞シートにおいて、上皮細胞のアピカル部が収縮し上皮細胞の形態を変化させる現象。上皮細胞シートが陥入する駆動力となる。神経管形成をはじめ、腸管形成にも関与している。(図2) - 密着結合(タイトジャンクション;TJ)
膜タンパク質クローディンにより隣り合う上皮細胞の間隙の距離をほぼ0にするほど密着させる細胞間接着装置。上皮細胞のアピカル側に上皮細胞を囲むように帯状に配置している。TJが形成されることで、上皮細胞シートは生体の外界と内界を隔てることが可能になり、これにより生体内の恒常性が保たれる。TJが破綻すると生体内の恒常性が崩れ、様々な病態を引き起こすことが知られている。(図3) - LUZP1
TJに局在する微小管タンパク質として同定した。LUZP1ノックアウトマウスでは神経管形成異常を呈する事が報告されていた。 - 上皮細胞シート
上皮細胞は、主にTJと接着結合(アドヘレンスジャンクション;AJ)が共同してAJC(apical junctional complex)として機能することにより、互いに側面で強く接着し、(2次元に広がる)上皮細胞シートを形成。 - アクトミオシンリング(circumferential ring: CR)
AJとTJからなるAJCと並行して配置されるアクチン繊維とミオシン繊維からなる構造体。AJCはAJやTJに局在するアクチン結合タンパク質を介してCRと相互作用している。 - 接着結合(アドヘレンスジャンクション;AJ)
膜タンパク質カドヘリンにより隣り合う上皮細胞を繋いでいる細胞間接着装置。TJの直下に配置され、TJと同様に上皮細胞を囲むように帯状に配置している。ただし、隣り合う上皮細胞の間隙として、20nm程の距離がある。 - ROCK1(Rho-associated, coiled-coil containing protein kinase 1)
低分子GTPaseであるRhoAの下流で働くセリンスレオニンキナーゼである。ROCK1がミオシン軽鎖をリン酸化する事でアクトミオシンが収縮する。
| 原著論文 | Embo J. e104712 (2020) |
|---|---|
| 論文タイトル | A microtubule-LUZP1 association around tight junction promotes epithelial cell apical constriction |
| 著者 | Tomoki Yano (1, 2), Kazuto Tsukita (2, 3), Hatsuho Kanoh (2, 4), Shogo Nakayama (2), Hiroka Kashihara (2), Tomoaki Mizuno (2), Hiroo Tanaka (2, 5, 6), Takeshi Matsui (7), Yuhei Goto (8, 9, 10), Akira Komatsubara (8, 9, 10), Kazuhiro Aoki (8, 9, 10), Ryosuke Takahashi (3), Atsushi Tamura (2, 5, 6), Sachiko Tsukita (2, 6)
|
| PubMed | 33346378 |
