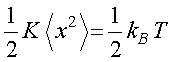
エネルギー等分配則,1分子計測にはとても必要な法則です.
バネの場合,
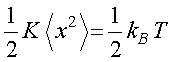
となるように,1自由度の持つ平均エネルギーは,1/2kBT,と表すことができます.
これは,運動エネルギー,位置エネルギーなどにも適用できます.
この求め方は,いろいろな方法があり,ここ,とかここ,などにも説明があります.
今回は,気体の運動エネルギーから求めてみましょう.
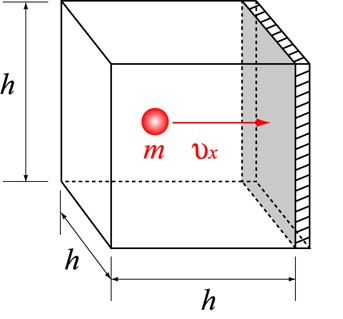
図のように,一辺の長さがh[m],体積がV(=h3) [m3],に一個の質量がm [kg]である理想気体が閉じ込められている空間を考えましょう.
ここでX軸に垂直な壁が、N個の気体分子から受ける圧力を考えます. 速度はX軸方向の速度のみを考えます.
ある一個の分子が壁に衝突するときの運動量の変化(力積)を考えます.
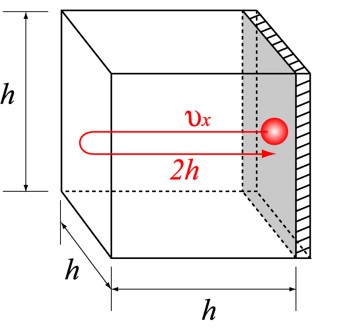
衝突前と後では,運動量の変化は,

のようになり,壁の衝突による運動量の変化は,
![]()
となります.
つまり,1回の衝突で気体分子が壁Aに与える力積(運動量の変化,力×時間 と等しい)は,2mvとなります.
さらに壁Aとの衝突は気体分子が1往復(2h[m])動くごとに1回起こ るから,t[s]間の衝突の回数は,
![]()
となります.
このため,壁Aが速度v[m/s]の気体分子からt[s]間に受ける 力積は,
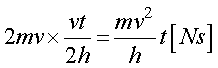
となります.
容器の中の気体分子の早さは乱雑なので、平均の速度を<v>とし, N個の気体分子によって壁Aがt[s]間に受ける力は,平均の力を<F> とすると,
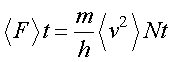
したがって,壁Aが気体分子から受ける圧力は受けた力Fを壁Aの面積,h2[m2],で割ればよいので,

となります.変形すると,
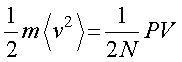
となります.
ここで,理想気体の状態方程式,
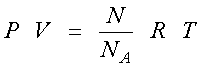
から,
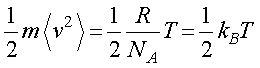
となり,等分配の法則を導き出すことができました.
ちなみに,酸素原子,O2,の場合,1分子の質量は,
![]()
となりますので,平均速度は,
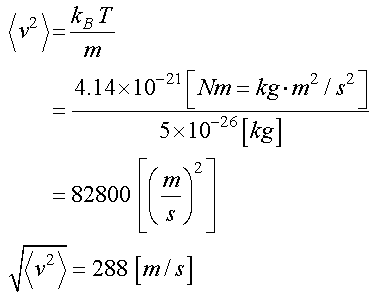
と約,秒速300m,時速1,000kmになることがわかります.
実際には他の分子と衝突して方向が変わるので,まっすぐ飛び続けるわけではありませんが...
次に,分子の運動エネルギーのボルツマン分布から求めてみましょう.