等吸収点
等吸収点とは,いろいろなサイト(ここ,ここ,など)で説明されていますが,私なりにまとめてみました.
(昔,プロジェクトの同僚に教えてもらった記憶があるのですが,もらった資料がどこかに行ってしまいました)
そもそも,吸収とは,ここ,に記載したように,
\( \Large A = \epsilon \ c \ x \)
ここで,
ε : モル分子吸光係数 (1/M 1/cm)
c : 溶液の濃度 (M)
x : 溶液の厚み (cm)
です.
この式は,ランベルト・ベールの法則,と呼ばれています.
分子吸光係数は波長に依存した値を取りますが,ここでは単純に一つのピークのガウス分布としておきます.
ある一次平衡反応を考えます.
\( \Large A \longleftrightarrow B \)
A状態とB状態で平衡状態となっています.
それぞれ,A,Bの物質には固有の吸光係数が存在するとします.
\( \Large A : \epsilon_A ( \lambda) \)
\( \Large B : \epsilon_B ( \lambda) \)

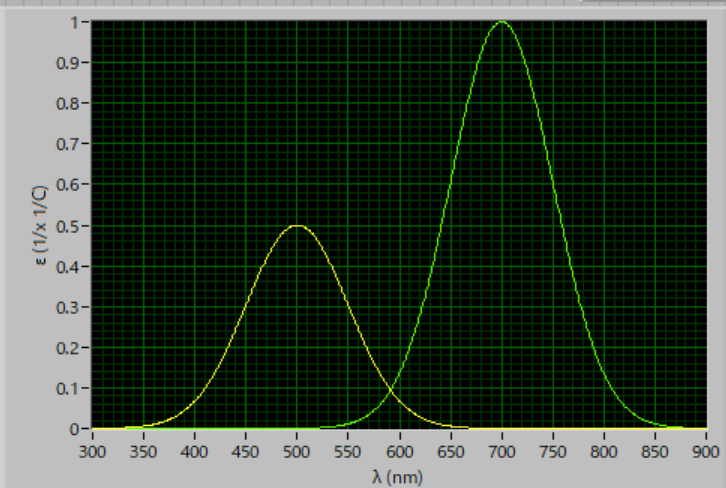
この適当に書いた吸光係数のカーブでは,それぞれの物質には最大となる吸光係数を取る波長(黄:500nm,緑:700nm)があり,ある程度の波長域に広がっています.
さらに,二つの吸光係数のカーブはある波長(λeq = 約580nm)で交差しています.
つまり,この波長では二つの吸光係数は等しい,ことになります.
AとBとの平衡反応ですので,それぞれの濃度の和は一定に保たれています.
\( \Large c_A + c_B = c_{total} = const \)
です.
このAとBとの混合液の吸収は,
\( \Large A = x \times [ \epsilon_A ( \lambda) \times c_A + \epsilon_B ( \lambda) \times c_B ] \)
となります.
ある環境(pHなど)でこの平衡状態における割合が変わるとしましょう.
それぞれの濃度は変化し,それぞれの吸光度は変化しますが,それぞれの濃度の和は一定です.
ここで,A,Bの吸光係数が等しい波長(λeq = 約580nm),を考えていきましょう.
吸光度が等しいので,
\( \Large \epsilon_A ( \lambda_{eq}) = \epsilon_B ( \lambda_{eq}) \equiv \epsilon_{eq} \)
となります.この波長での吸収は,
\( \Large \begin{eqnarray} A &=& x \times [ \epsilon_{eq} \times c_A + \epsilon_{eq} \times c_B ] \\
&=&
x \times \epsilon_{eq} \times [c_A + c_B ] \\
&=&
x \times \epsilon_{eq} \times c_{total} \\
\end{eqnarray} \)
となり,常に一定の値となります.この波長を,等吸収点,と呼びます.
従って,環境の変化でAとBの存在比が変化しても,同じ吸光なので,一点に交わることになります.
実査にシミュレーションしてみました.
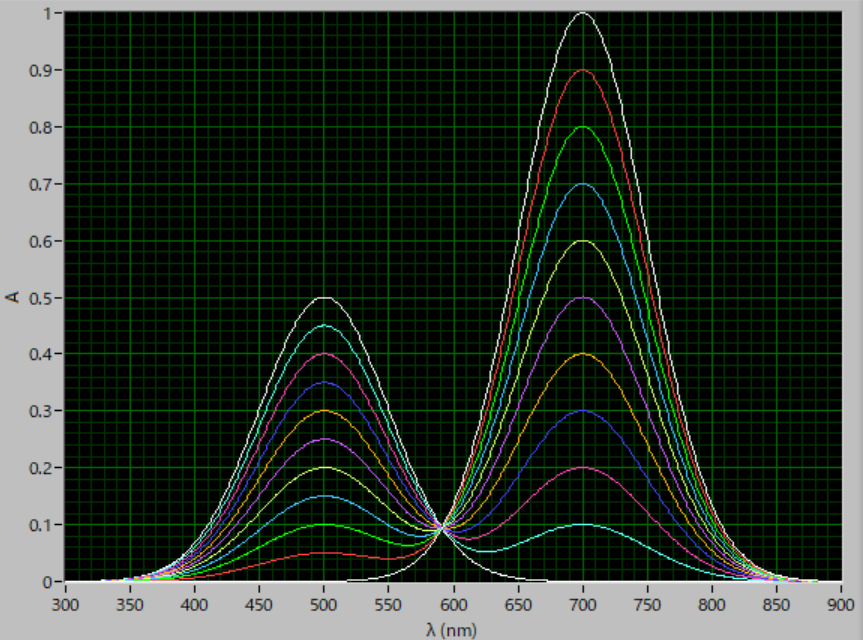
このようにAとBの存在比を変化させても,きれいな一点で交わることが分かります.
この等吸収点で重要な点は,
二種類の物質の一次反応のみ適応できる
と言う点です,逆に言うと,等吸収点が実験から見られたら,その反応は二種類の物質の一次反応である,と言うことが言えます.
逐次反応などになると,等吸収点は見られない(はず)です.